Une polyradiculonévrite inflammatoire démyélinisante chronique paranéoplasique secondaire à un lymphome natural killer nasal
Selim Jennane, Nawal Hasnaoui, Mahtat El Mehdi, Hicham El Maaroufi, Nezha Messaoudi, Mohamed Mikdame, Kamal Doghmi
Corresponding author: Selim Jennane, Service d'Hématologie Clinique, Hôpital Militaire d'Instruction Mohammed V, Université Mohammed V, Rabat, Maroc 
Received: 25 Nov 2018 - Accepted: 24 Jul 2020 - Published: 18 Aug 2020
Domain: Oncology,Neurology (general)
Keywords: Lymphome, polyradiculonévrite, paranéoplasique
©Selim Jennane et al. Pan African Medical Journal (ISSN: 1937-8688). This is an Open Access article distributed under the terms of the Creative Commons Attribution International 4.0 License (https://creativecommons.org/licenses/by/4.0/), which permits unrestricted use, distribution, and reproduction in any medium, provided the original work is properly cited.
Cite this article: Selim Jennane et al. Une polyradiculonévrite inflammatoire démyélinisante chronique paranéoplasique secondaire à un lymphome natural killer nasal. Pan African Medical Journal. 2020;36:303. [doi: 10.11604/pamj.2020.36.303.17772]
Available online at: https://www.panafrican-med-journal.com//content/article/36/303/full
Case report 
Une polyradiculonévrite inflammatoire démyélinisante chronique paranéoplasique secondaire à un lymphome natural killer nasal
Une polyradiculonévrite inflammatoire démyélinisante chronique paranéoplasique secondaire à un lymphome natural killer nasal
Chronic paraneoplastic inflammatory demyelinating polyradiculoneuritis secondary to nasal natural killer lymphoma
Selim Jennane1,&, Nawal Hasnaoui1, Mahtat El Mehdi1, Hicham El Maaroufi1, Nezha Messaoudi2, Mohamed Mikdame1, Kamal Doghmi1
&Auteur correspondant
Nous rapportons un cas unique d´une polyradiculonévrite inflammatoire démyélinisante chronique paranéoplasique secondaire à un lymphome non hodgkinien T de type natural killer nasal.
We here report a single case of chronic paraneoplastic inflammatory demyelinating polyradiculoneuritis secondary to a nasal natural killer (NK) non-Hodgkin T lymphoma.
Key words: Lymphoma, polyradiculoneuritis, paraneoplastic
La polyradiculonévrite inflammatoire démyélinisante chronique (PIDC) paranéoplasique est une complication rare décrite dans différentes pathologies néoplasiques. Son association avec un lymphome non hodgkinien T (LNHT) de type natural killer (NK) nasal n´a jamais été rapporté par la littérature.
Un patient de 52 ans, sans antécédent, a été admis dans notre formation pour l´exploration d´une altération de l´état général. A l´interrogatoire le patient présentait depuis trois mois, une faiblesse symétrique des muscles proximaux et distaux des quatre membres, d´aggravation progressive, ainsi que des douleurs neuropathiques au niveau des membres inférieurs. Il se plaignait aussi de l´apparition récente d´une dysphagie et d´une dysphonie ainsi qu´une perte de poids estimée à 10 kg en 3 mois. L´examen neurologique retrouvait un déficit moteur symétrique des muscles proximaux et distaux des quatre membres. La sensibilité était altérée et les réflexes ostéo-tendineux étaient absents aux membres inférieurs et diminués au niveau des membres supérieurs.
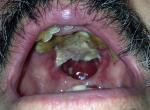
L´examen des nerfs crâniens était sans anomalie. L´examen de la cavité buccale montrait la présence d´une masse nécrosée qui perforait le palais dure et qui entrainait une communication entre la cavité nasale et la cavité buccale (Figure 1). L´électro neuro myogramme réalisé sur plusieurs nerfs décelait l´existence d´un bloc de conduction partiel des nerfs moteurs, un ralentissement de la vitesse de conduction des nerfs moteurs ainsi qu´un allongement de la latence motrice distale et des latences des ondes F. La ponction lombaire montrait une hyper protéinorachie à 3g/l sans hyper leucorachie (4 cellules/mm³). La biopsie de la masse nasale était en faveur d´un lymphome non hodgkinien T de type NK nasal. Le bilan d´extension ne retrouvait pas de localisation secondaire. L´imagerie par résonnance magnétique (IRM) cérébrale était sans anomalie. Les sérologies de l´hépatite B et C et du virus d´immunodéficience humaine (VIH) étaient négatives. La fonction rénale et le bilan hépatique étaient normaux.
Il n´existait pas de gammapathie monoclonale à l´électrophorèse des protéines sériques. Le diagnostic retenu était celui d´une polyradiculonévrite inflammatoire démyélinisante chronique paranéoplasique secondaire à un LNHT de type NK nasal. Le patient a reçu deux cures de chimiothérapie comportant la dexaméthasone, la L-asparginase ainsi que le méthotrexate entrainant une amélioration rapide mais partielle du déficit neurologique. Il a ensuite bénéficié d´une radiothérapie locale suivie de deux autres cures de chimiothérapie selon le même protocole. L´évolution était marquée initialement par l´obtention d´une réponse partielle estimée à 90% selon les critères de Cheson et al. [1]. A 3 mois de la fin du traitement le patient a présenté une progression du volume de la masse ainsi qu´une aggravation de la symptomatologie neurologique. Il est décédé à 11 mois du diagnostic.
Selon notre recherche sur « PubMed », notre patient est le premier cas décrit dans la littérature d´une PIDC secondaire à un LNHT de type NK nasal. Les PIDC sont un groupe hétérogène de neuropathies démyélinisantes auto-immunes acquises [2]. L´origine auto immune des PIDC a été évoquée par la présence des lymphocytes T et d´un infiltrat macrophagique phagocytant les débris myéliniques, dans l´endonèvre des biopsies nerveuses [3]. Ce phénomène a été ensuite conforté à l´aire des anticorps par la mise en évidence d´anticorps dirigés contre les différentes structures nerveuses [4]. Comme dans notre observation le diagnostic repose sur un faisceau d´arguments cliniques, biologiques et électrophysiologiques. Les critères utilisés actuellement sont ceux du groupe de travail conjoint de l´European Federation of Neurological Societies (EFNS) et de la Peripheral Nerve Society (PNS) [5].
Les PIDC sont souvent idiopathiques [6]. Dans certains cas, elles peuvent être secondaires ou accompagner diverses pathologies. Les causes infectieuses sont dominées les hépatites C et B, le VIH et la maladie de Lyme [6]. Parmi les maladies systémiques associées à la PIDC on distingue le lupus, la sarcoïdose, les thyroïdites auto immunes, les hépatites auto-immunes, la cryoglobulinémie, la polyarthrite rhumatoïde et le syndrome de Gougerot Sjögren [6]. En présence d´une gammapathie monoclonale, il est indispensable de vérifier si celle-ci possède une activité anticorps (anti-MAG, anti-GQ1b) et de rechercher une maladie de Waldenstrom, un myélome multiple, un syndrome de POEMS (Polyneuropathy, Organomegaly, Endocrinopathy, Monoclonal protein and Skin changes), avant de conclure à une gammapathie monoclonale de signification indéterminée (MGUS) [7, 8]. Le lien entre le PIDC et certaines pathologies reste controversé comme chez les patients atteints d´un diabète [9], d´une maladie inflammatoire chronique de l'intestin (MICI) et de certaines vascularites [7]. Une cause néoplasique doit être évoquée devant un amaigrissement, des signes généraux ou un syndrome tumoral. Plusieurs cancers solides ont été incriminés dans les PIDC dont les cancers pulmonaires, les mélanomes et les lymphomes hodgkinien et non hodgkinien [10, 11]. En plus de l´atteinte du système nerveux central par l´envahissement tumorale, les lymphomes B et T peuvent être responsable de diverses neuropathies périphériques par des mécanismes immunologiques mal élucidés [12, 13]. Les lymphomes B sont plus souvent responsables de neuropathie périphériques que les LNHT [10].
Sur le plan thérapeutique, notre choix était basé sur les études récentes montrant la supériorité des protocoles de chimiothérapie comportant la L-asparginase couplés à une radiothérapie en « sandwich » [14]. L´état général du patient ne permettait pas l´utilisation d´un protocole plus agressif.
Au cours d´une hémopathie maligne, le diagnostic d´une PIDC paranéoplasique doit être évoqué devant tout déficit moteur ou sensitif et confirmé par un faisceau d´arguments cliniques, biologiques et électromyographiques.
Les auteurs ne déclarent aucun conflit d'intérêts.
Tous les auteurs ont contribué à la gestion du patient, à la recherche bibliographique, à la rédaction du manuscrit ainsi qu´à son approbation. Tous les auteurs ont lu et approuvé la version finale du manuscrit.
Figure 1: masse nécrosée, détruisant le palais osseux et créant une communication entre la cavité nasale et la cavité buccale
- Cheson BD, Pfistner B, Juweid ME, Gascoyne RD, Specht L, Horning SJ et al. Revised response criteria for malignant lymphoma. J Clin Oncol. 2007 Feb 10;25(5):579-86. PubMed | Google Scholar
- Rajabally YA, Simpson BS, Beri S, Bankart J, Gosalakkal JA. Epidemiologic variability of chronic inflammatory demyelinating polyneuropathy with different diagnostic criteria: study of a UK population. Muscle Nerve. 2009 Apr;39(4):432-8. PubMed | Google Scholar
- Bouchard C, Lacroix C, Planté V, Adams D, Chedru F, Guglielmi JM et al. Clinicopathologic findings and prognosis of chronic inflammatory demyelinating polyneuropathy. Neurology. 1999 Feb;52(3):498-503. PubMed | Google Scholar
- Mathey EK, Park SB, Hughes RA, Pollard JD, Armati PJ, Barnett MH et al. Chronic inflammatory demyelinating polyradiculoneuropathy: from pathology to phenotype. J Neurol Neurosurg Psychiatry. 2015 Sep;86(9):973-85. PubMed | Google Scholar
- Joint Task Force of the EFNS and the PNS. European Federation of Neurological Societies/Peripheral Nerve Society Guideline on management of chronic inflammatory demyelinating polyradiculoneuropathy: report of a joint task force of the European Federation of Neurological Societies and the Peripheral Nerve Society? first revision. J Peripher Nerv Syst. 2010 Sep;15(3):185-95. PubMed | Google Scholar
- Viala K. Epidemiological and clinical aspects of CIDP. Rev Neurol (Paris). 2007 Sep;163 Spec No 1:3S31-5. PubMed | Google Scholar
- French CIDP Study group. Recommendations on diagnostic strategies for chronic inflammatory demyelinating polyradiculoneuropathy. J Neurol Neurosurg Psychiatry. 2008 Feb;79(2):115-8. PubMed | Google Scholar
- Viala K, Maisonobe T, Stojkovic T, Koutlidis R, Ayrignac X, Musset L et al. A current view of the diagnosis, clinical variants, response to treatment and prognosis of chronic inflammatory demyelinating polyradiculoneuropathy. J Peripher Nerv Syst. 2010 Mar;15(1):50-6. PubMed | Google Scholar
- Kalita J, Misra UK, Yadav RK. A comparative study of chronic inflammatory demyelinating polyradiculoneuropathy with and without diabetes mellitus. Eur J Neurol. 2007 Jun;14(6):638-43. PubMed | Google Scholar
- Antoine JC, Camdessanche JP. Les neuropathies périphériques paranéoplasiques. Rev Neurol (Paris). 2004 Feb;160(2):188-98. PubMed | Google Scholar
- Antoine JC, Mosnier JF, Lapras J, Convers P, Absi L, Laurent B et al. Chronic inflammatory demyelinating polyneuropathy associated with carcinoma. J Neurol Neurosurg Psychiatry. 1996 Feb;60(2):188-90. PubMed | Google Scholar
- Griggs JJ, Commichau CS, Rapoport AP, Griggs RC. Chronic inflammatory demyelinating polyneuropathy in non-Hodgkin's lymphoma. Am J Hematol. 1997 Apr;54(4):332-4. PubMed | Google Scholar
- Wada M, Kurita K, Tajima K, Kawanami T, Kato T. A case of inflammatory demyelinating polyradiculoneuropathy associated with t-cell lymphoma. Acta Neurol Scand. 2003 Jan;107(1):62-6. PubMed | Google Scholar
- Tse E, Kwong YL. How I treat NK/T-cell lymphomas. Blood. 2013 Jun 20;121(25):4997-5005. PubMed | Google Scholar