Alloimmunisation fśto-maternelle Rhésus grave ŕ propos d’un cas et revue de la littérature
Benkerroum Zineb, Lachiri Boutaina, Lazrak Ikram, Moussaoui Rahali Driss, Dehayni Mohammed
Corresponding author: Benkerroum Zineb, Service de Gynécologie Obstétrique, Hôpital Militaire d’instruction Mohammed V, Avenue des Far Hay Riad, Rabat, Maroc 
Received: 22 Oct 2013 - Accepted: 06 Jun 2014 - Published: 14 Oct 2015
Domain: Maternal and child health
Keywords: Alloimmunisation, anasarque fśtal, pic systolique, transfusion in utéro, prophylaxie
©Benkerroum Zineb et al. Pan African Medical Journal (ISSN: 1937-8688). This is an Open Access article distributed under the terms of the Creative Commons Attribution International 4.0 License (https://creativecommons.org/licenses/by/4.0/), which permits unrestricted use, distribution, and reproduction in any medium, provided the original work is properly cited.
Cite this article: Benkerroum Zineb et al. Alloimmunisation fśto-maternelle Rhésus grave ŕ propos d’un cas et revue de la littérature. Pan African Medical Journal. 2015;22:137. [doi: 10.11604/pamj.2015.22.137.3508]
Available online at: https://www.panafrican-med-journal.com//content/article/22/137/full
Original article 
Alloimmunisation fśto-maternelle Rhésus grave ŕ propos d’un cas et revue de la littérature
Alloimmunisation fśto-maternelle Rhésus grave ŕ propos d’un cas et revue de la littérature
Benkerroum Zineb1,&, Lachiri Boutaina1, Lazrak Ikram1, Moussaoui Rahali Driss1, Dehayni Mohammed1
1Service de Gynécologie Obstétrique, Hôpital Militaire d’instruction Mohammed V, Avenue des Far Hay Riad, Rabat, Maroc
&Auteur correspondant
Benkerroum Zineb, Service de Gynécologie Obstétrique, Hôpital Militaire d’instruction Mohammed V, Avenue des Far Hay Riad, Rabat, Maroc
L’incompatibilité fśto-maternelle Rhésus peut ętre ŕ l’origine d’un syndrome hémolytique dont l’expression clinique est l´anémie fśtale éventuellement compliquée par une anasarque fśto-placentaire ou ŕ l’extręme une mort fśtale in utéro. Nous rapportons l’observation d’un cas d’allo immunisation Rhésus ŕ 34 SA ayant aboutit un hydrops foetalis, l’extraction fśtale par césarienne en vue d’une exsanguino-transfusion a été réalisée, mais le nouveau né est décédé au cours de l’exsanguino-transfusion. Le dépistage des femmes ŕ risque et l’utilisation d’Immunoglobulines anti D ont permis une réduction importante de l´incidence des accidents d’incompatibilité. La mesure du pic systolique de vélocité dans l’artčre cérébrale moyenne a bouleversé la surveillance et la prise en charge prénatale des anémies fśtales secondaires ŕ une allo-immunisation Rhésus. Son utilisation dans la surveillance des cas d’allo-immunisation Rhésus permettrait ainsi de réserver les procédures invasives (cordocentčse) comme geste thérapeutique qui permet la transfusion fśtale in utéro. Grâce ŕ une collaboration multidisciplinaire cohérente, l’extraction fśtale peut ętre programmée, ce qui permet une prise en charge adéquate et rigoureuse, męme des nouveaux nés avec atteinte sévčre.
L’allo-immunisation fśto-maternelle dans le systčme RH est la premičre cause d’anémie fśtale néonatale. Elle est responsable d’un syndrome hémolytique fśtal de gravité variablequi se manifeste in utéro par un état d’anasarque pouvant aller jusqu’ŕ la mort fśtale in utéroet ŕ la naissance d’un ictčre hémolytique. La situation la plus classique de l’allloimmunisationfoeto-maternelle concerne l’antigčne D[1]. Cependant, des phénomčnes d’alloimmunisation peuvent survenir dans d’autres groupes érythrocytaires[2]. Bous rapportons l’observation d’un cas d’alloimmunisation fśto-maternelle dans le systčme RHayant aboutit ŕ un décčs néonatal au cours de l’exsanguino-transfusion dans un contexte d’anasarque fśto-placentaire.
Une patiente de 41 ans, G4P3, 1 enfants vivant, de groupe AB Rh-, la premičre grossesse c’est soldé par un accouchement par voie basse d’un nouveau né vivant mais l’anti D n’a pas été reçu, les deux autres grossesses ont été marquées par un décčs néonatal respectivement ŕ j7 et J1 de vie, dans un contexte d’ictčre hémolytique.
La quatričme grossesse est la grossesse actuelle, était mal suivie. La patiente était vue en consultation prénatale pour la premičre fois ŕ 32SA oů elle avait bénéficié d’une échographie obstétricale qui a objectivé une anasarque foeto-placentaire et adressée ŕ notre formation pour prise en charge. Elle a consulté dans notre formation ŕ 34 SA. A l’examen clinique la hauteur utérine était excessive ŕ 31cm avec un ballotement fśtal perceptible ŕ la palpation abdominale, les bruits cardiaques fśtaux étaient réguliers mais sourds.
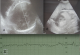
L’échographie obstétricale a objectivé une grossesse évolutive en présentation de sičge. La biométrie fśtale correspondait ŕ l’âge gestationnel pour le diamčtre bipariétal (BIP= 87mm) et pour la longueur du fémur (LF=66mm). Cependant la circonférence abdominale était supérieure au 90čme percentile de 34SA (CA=423mm). Le fśtus était en état d’anasarque avec présence d’épanchement pleural bilatéral, péricardique et une ascite ainsi qu’un śdčme sous cutané diffus (Figure 1 A et B). L’exploration des viscčres avait objectivé une hépatomégalie. La veine ombilicale était dilatée mesurant 11mm. Le placenta était épaissi mesurant 80mm. L’hydramnios était manifeste avec un index du liquide amniotique ŕ 350mm. Le doppler ombilical était normal avec un indexe de résistance ŕ 0,64 et le doppler cérébral a montré une élévation du pic systolique de vélocitémesuré sur l’artčre cérébrale moyenne arrivant ŕ 80 cm/s. Le rythme cardiaque fśtal était franchement pathologique de type sinusoďdal (figure 1 C).Sur le bilan biologique la recherche d’agglutinines irréguličres était positive, cependant le titrage n’a pu ętre réalisé.
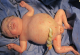
La césarienne a été réalisée le jour męme, elle a permis l’extraction d’un nouveau-né vivanten hydrops fśtalis (Figure 2), le score Apgarétait ŕ 5/10 ŕ la naissance et ŕ 5min. L’hémogramme et la demande de culots globulaire ont été réalisés su sang du cordon. Le nouveau-né était hypotonique trčs peu réactif, avec respiration spontanée irréguličre et un rythme cardiaque fśtal ŕ 120 bpm. Il présentait ŕ la naissance des śdčmes étendus et une distension abdominale importante, sans ictčre cutané. Il a été intubé et ventilé et transféré en réanimation. En réanimation, un cathéter ombilical a été posé afin de réaliser une exsanguino-transfusion. Il a été réalisé également une ponction pleurale bilatérale. Le taux d’hémoglobine était ŕ 6g/dl. Au moment de commencer l’exsanguino transfusion, le nouveau né a présenté un arręt cardio-circulatoire non récupéré. Il est décédé ŕ H1 de vie.
Physiopathologie – Étiologie
Le systčme Rhest constitué de deux gčnes contigusRHD et RHCE présents sur le chromosome 1. Le gčne RHD code pour la protéine D (RH1) qui constitue le groupe RhD positif (RH: 1) au sujet qui la possčde.Les individus ne possédant pas le gčne RHD sont doncRhD négatif (RH: -1).Le second gčne RHCE porte les antigčnes C (RH2), E(RH3), c (RH4) et e (RH5) en formant quatre combinaisonsCE, Ce, cE, ce [3].
La séquence des événements qui aboutit ŕ l’alloimmunisation fśto-maternelle se déroule selon les étapes suivantes: 1) passage d’hématies fśtales ŕ travers le placenta; 2) réponse immunitaire primaire maternelle; 3) réponse immunitaire secondaire, habituellement lors d’une grossesse ultérieure, lorsque le fśtus exprime l’antigčne RhD produisant des immunoglobuline de type IgG; 4) passage des IgG ŕ travers le placenta et fixation sur les hématies foetales; 5) déclenchement de la maladie hémolytique avec ses conséquencespour le fśtus ou pour le nouveau-né. Les macrophages de la rate et du foie qui vont capter les globules rouges fśtaux fixant les IgG-antiD, entrainant leur hémolyse intra tissulaire et par conséquent une anémie fśtale de gravité variable. Des phénomčnes de compensation seront déclenchés pour lutter contre l’anémie fśtale; L’érythropoďčse accru dans les tissus hématopoďčtique (Foie, rate) vont entrainer un dysfonctionnement hépatique (hypoalbuminémie) et une hypertension portale également de gravité variable aboutissant au tableau classique d’hydrops foetalis avec épanchement des séreuses, śdčme cutané diffus, hépato-splénomégalie, hydramnios et épaississement placentaire [3]. A la naissance, l’immaturité du foie fśtal limite la conjugaison de la bilirubine produite lors de l’hémolyse. Son accumulation dans la circulation fśtale entraine un ictčre néonatal secondaire responsable d’ictčre nucléaire.
Cette succession d’événements concerne donc au moins deux contacts antigéniques dans cette forme habituellede la maladie. Le premier contact s’effectue au cours de la premičre grossesse ou de l’accouchement; car il existe un passage physiologique de quelques globules rouges fśtaux dans la circulation maternelle. Ce passage est augmenté parallčlement avec l’âge de la grossesse [3], lors des interventions ou traumatisme sur utérus gravide et lors des métrorragies. En dehors de la grossesse, les transfusions de produits sanguins sont devenues actuellement des situations exceptionnelles d’allo immunisation.
Le dépistage des grossesses ŕ risque d’alloimmunisation:
Commence par la détermination du groupe sanguin de la mčre en début de grossesse, ainsi que celui du pčre en cas de mčre Rh:-1. Il est actuellement possible de réaliser une détermination du groupe sanguin fśtal dans le sang maternel dčs la 10čme SA par PCR.
La recherche des agglutinines irréguličres (RAI) est la technique de choix pour la surveillance des grossesses ŕ risque. En effet, l’absence d’agglutinine irréguličre élimine toute atteinte fśtale. Toutes les femmes enceintes doivent bénéficier d’une recherche des agglutinines irréguličre en début de grossesse. Pour les femmes de groupe Rh:-1, cet examen doit ętre répété chaque mois [2]. La positivisation des RAI au cours de la grossesse témoigne de la survenue d’alloimmunisation dont il faut apprécier la gravité.
La titration des agglutinine irréguličre est réalisée dčs que la recherche des agglutinine irréguličre est positive. Au delŕ d’un titre de 8, Il est préférable de réaliser un dosage pondéral des anticorps. Cependant ce dosage n’est valable que pour les immunisations dans le systčme Rh:1. Il existe une certaine corrélation entre ces deux examens et le degré de gravité de l’immunisation [4]. En effet, le risque d’atteinte fśtal est minime si le titre est inférieur ŕ 16 et si le dosage pondéral est inférieur ŕ 1µg/ml. Un dosage pondéral supérieur ŕ 5µg/ml témoigne d’une atteinte fśtale sévčre [3]. Le rythme de surveillance biologique des grossesses conflictuelles dépend de la sévérité de l’atteinte; si le titre reste inférieur ŕ 16, une titration est réalisée chaque mois puis chaque deux semaine ŕ la deuxičme moitié de la grossesse [4].
L’évaluation de la sévérité de l’atteinte fśtale
L’appréciation du degré de l’anémie fśtal a été révolutionnée par la mesure du pic systolique de vélocité de l’artčre cérébrale moyenne (ACM) au doppler [5]. Contrairement aux méthodes invasives; amniocentčse et cordocentčse, La mesure du pic systolique de vélocité de l’ACM et une technique non invasive reproductible, ayant une sensibilité de 91% et une spécificité de 100% dans la détection des anémies fśtales sévčres [6]. L’augmentation du pic systolique de L’ACM serait due ŕ l’augmentation du débit cardiaque et ŕ la diminution de la viscosité sanguine par diminution de l’hématocrite fśtale [6, 7]. En effet, le risque d’anémie fśtale sévčre est accru si le pic systolique de vélocité de l’ACM est supérieur au 1,5 multiple de la médiane (MoM) pour le męme âge gestationnel projetée sur la courbe de Mari. Le rythme de surveillance par le doppler est variable en fonction de la sévérité de l’atteinte. Une surveillance bimensuelle au delŕ de 20 SA si l’immunisation est modérée. La surveillance est hebdomadaire si le risque d’anémie fśtale est plus important avec dosage bimensuel des anticorps [8].
L’échographie fśtale recherche les signes d’intolérance fśtale ŕ l’anémie; l‘hydramnios, l’anasarquefśto-placentaire et l’hépato-splénomégalie qui sont des signes tardifs prédicteur d’anémie fśtale sévčre, contrairement ŕ la mesure de l’épaisseur du placenta et de la veine ombilicale [7].
L’étude du rythme cardiaque fśtal permet la surveillance du bien ętre fśtal dčs que les signes d’anémies fśtale. Les anomalies sont variables, et réalisent ŕ l’extręme un rythme sinusoďdal.
Les procédés invasifs intraovulairessont actuellement réservés ŕ une visée thérapeutique.
La prise en charge thérapeutique doit débuter en anténatal, la décision de transfusion in utéro est envisageable dčs 17 SA-20SA jusqu´ŕ 34 SA [3]. Il s’agit d’un geste invasif qui consisté ŕ ponctionner in utéro la veine coronale et ŕ transfuser des globules rouges irradiés de groupe O et de phénotype identique ŕ celui maternel. Avant la transfusion, l’anémie doit ętre confirmée par un dosage direct sur le sang fśtal. Ce procédé n’est pas dénué de risque, de mort fśtale in utéro ou d’accouchement prématuré évalué ŕ 3% [8]. Il peut s’agir d’une transfusion in utéro simple (TIU) ou avec soustraction du sang fśtal. L’exsanguino-transfusion in utéro (ETIU) ŕ l’avantage de limiter la surcharge volémique fśtale mais elle expose ŕ un risque fśtal plus important limitant son utilisation [8]. L’extraction fśtale,en cas d’atteinte sévčre, est programmée dčs que le risque de grande prématurité est écarté. Pour les attentes modérées et légčre il n’y a aucun intéręt ŕ maintenir la grossesse au delŕ du terme de 37 SA, car le risque d’aggravation brutale existe toujours.
La prise en charge postnatale est axée sur deux principaux paramčtres; la correction de l’anémie fśtale et del’hyperbilirubinémie. La réalisation de photothérapie précoce et intensive permet de réduire le taux de bilirubine fśtale. La transfusion fśtale est indiquéeencas d’anémie fśtale mal tolérée. L’exsanguino transfusion est réservée aux cas d’anasarque avec anémie profonde et d’hyperbilirubinémie menaçante d’ictčre nucléaire résistante au traitement par photothérapie [9]. Le recours ŕ l’exsanguino-transfusion a régressé depuis l’élargissement des transfusions fśtales in utéro.
La prophylaxie
L’application stricte des mesures de prophylaxie par injection d’immunoglobuline anti-D a permis de réduire l’incidence de l’alloimmunisation fśto-maternelle. Elle répond ŕ des standards réguličrement actualisés. Le collčge national des gynécologues et obstétriciens français recommande depuis 2005 l’utilisation d’immunoglobuline anti D chez les patientes Rhésus négatif chez qui la recherche d’agglutinines irréguličres est négative selon un protocole bien établi. Au cours de la grossesse, l’injection de 200µg d’immunoglobuline anti D n’est réalisée qu’aprčs un incident favorisant le passage de globules rouges fśtales ŕ la circulation maternelle au premier et au deuxičme trimestre. Au troisičme trimestre de la grossesse l’injection de 300µg d’immunoglobuline anti-D est systématique ŕ 28 SA. Aprčs l’accouchement une injection de 200µg d’immunoglobuline anti-D est administrée systématiquement aprčs la naissance, une dose supplémentaire sera administrée ultérieurement en fonction du résultat du test de Kleihauer et aprčs vérification du groupe sanguin fśtal [3].
L’allo-immunisation fśto-maternelle anti-érythrocytaire reste d’actualité du fait de leur persistance malgré les mesures prophylactiques et du fait des progrčs considérables dans les méthodes de prise en charge.
Les auteurs ne déclarent aucun conflit d’intéręts.
Tous les auteurs ont lu et approuvé la version finale du manuscrit.
Figure 1: A) image échographique de la tęte fśtale montrant un śdčme du scalp (flčche); (B) image échographique montrant l’ascite de grande abondance (flčche) sur une coupe sagittale de
l’abdomen; (C) enregistrement du rythme cardiaque fśtal de type sinusoďdal
Figure 2: le nouveau né en hydrops foetalis
- Guigonis V, Debiec H, Deschęnes G, Bensman A, Ronco P. Allo-immunisation maternofoetale tissulaire: nouvelles cibles antigéniques, nouvelles idées. Archives de pédiatrie. 2006; 13(1):4–5. PubMed | Google Scholar
- Gariod S, Brossard Y, Poissonnier MH, Vuilliez B, Deutsch V, Jouk PS, Pons JC, Gariod S. Allo-immunisation anti-Kell et grossesse. J GynecolObstetBiolReprod. 2004; 33(7):637-648. PubMed | Google Scholar
- Rigala D, Meyera F, Mayranda E, Dupraza F. Les allo-immunisations foeto-maternelles anti-érythrocytaires: état de l’art en 2008. Revue francophone des laboratoires. 2008; 2008(402):51-62. PubMed | Google Scholar
- Bricca P, Guinchard E, Guitton Bliem C. Prise en charge des allo-immunisationsfoeto-maternelles anti-érythrocytaires. Transfusion Clinique et Biologique. 2011; 18(2):269—276. PubMed | Google Scholar
- Mari G et al. Noninvasivediagnosis by doppler ultrasonography of fetalanemia due to maternalred-cellalloimmunization. N Engl J Med. 2000; 342(1):9-14. PubMed | Google Scholar
- Oppenheimer A, Jouannic JM, Carbonne B, Brodaty G, Renolleau S, Bénifla JL. Apport de la mesure du pic des vitesses systoliques dans l’artčre cérébrale moyenne pour la discussion étiologique des anasarques fśtaux. J GynecolObstetBiolReprod. 2006; 35(2):176-180. PubMed | Google Scholar
- Brennand J. Fetalanaemia: diagnosis and management. Best Practice &ResearchClinicalObstetrics and Gynaecology. 2008; 22(1):15–29. PubMed | Google Scholar
- Carbonne B, Castaigne V, Cynober E, Levy R, Cortey A, Mailloux A, Larsen M, Brossard Y. Le point sur le suivi des allo-immunisationsérythrocytaires. Gynécologie Obstétrique & Fertilité. 2010; 38(3):205–213. PubMed | Google Scholar
- Hascoet JM, Hamon I, Morel O, Miton I,Knebi MT. Prise en charge néonatale des allo-immunisationsRhésus sévčres aprčs exsanguino-transfusion inUtero: vers une nouvelle stratégie. Les JTA. http://www.lesjta.com/article.php?ar_id=1100. Accessed 11th June 2014. PubMed | Google Scholar