Réactions immunoallergiques graves aux antibacillaires: ŕ propos de 10 cas
Sabah El Machichi Alami, Sanae Hammi, Jamal Eddine Bourkadi
Corresponding author: Sabah El Machichi Alami, Hôpital Moulay Youssef, CHU, Rabat, Maroc 
Received: 19 Aug 2014 - Accepted: 02 Sep 2014 - Published: 15 Oct 2014
Domain: Clinical medicine
Keywords: Tuberculose, traitement antibacilaire, effet secondaire, réaction immunoallergique grave
©Sabah El Machichi Alami et al. Pan African Medical Journal (ISSN: 1937-8688). This is an Open Access article distributed under the terms of the Creative Commons Attribution International 4.0 License (https://creativecommons.org/licenses/by/4.0/), which permits unrestricted use, distribution, and reproduction in any medium, provided the original work is properly cited.
Cite this article: Sabah El Machichi Alami et al. Réactions immunoallergiques graves aux antibacillaires: ŕ propos de 10 cas. Pan African Medical Journal. 2014;19:152. [doi: 10.11604/pamj.2014.19.152.5225]
Available online at: https://www.panafrican-med-journal.com//content/article/19/152/full
Réactions immunoallergiques graves aux antibacillaires: ŕ propos de 10 cas
Sabah El Machichi Alami1,&, Sanae Hammi1, Jamal Eddine Bourkadi1
1Hôpital Moulay Youssef, CHU, Rabat, Maroc
&Auteur correspondant
Sabah El Machichi Alami, Hôpital Moulay Youssef, CHU, Rabat, Maroc
L'hypersensibilité aux antituberculeux est l'un des effets secondaires imprévisibles qui apparait chez 4 ŕ 5 % de la population exposée et s'élčve ŕ 25% chez les sujets VIH positifs. Dans notre étude parmi 39 patients ayant présenté des réactions immunoallergiques, 10 avaient des formes graves. Le délai moyen d'apparition des signes était de 23 jours. Les réactions immunoallergiques observées étaient 5 cas de toxidermie généralisée fébrile, un cas de Dress syndrome, un cas de neutropénie, un cas de pancitopénie et 2 cas de thrombopénie. Tous nos patients avaient bien évolué cliniquement et bactériologiquement aprčs l'adoption d'un régime thérapeutique excluant le ou les médicaments incriminés. En pratique, si l'effet indésirable imputé ŕ un antituberculeux est grave, il est impératif de l'arręter, de traiter l'incident et d'associer une autre molécule chez certains cas. Notre étude a montré une fréquence significative des complications graves probablement sous-estimée, surtout dans les pays fortement touchés par l'infection HIV.
Les allergies médicamenteuses peuvent ętre définies comme des réactions pathologiques induites par une prise médicamenteuse liées ŕ un mécanisme immunologique [1]. L'hypersensibilité aux antituberculeux est l'un des effets secondaires imprévisibles qui apparait chez 4 ŕ 5% de la population exposée et s'élčve ŕ 25% chez les sujets VIH positifs [1,2].
Etude rétrospective menée ŕ l'hôpital Moulay Youssef de Rabat s'étalant sur une période de 18 mois (2013-2014). L'objectif était de recenser les patients ayant présenté des réactions immunoallergiques graves aux antibacillaires au cours de leur hospitalisation.
Parmi 39 patients ayant présenté des réactions immunoallergiques, 10 avaient des formes graves (25.6%). L'âge moyen de nos patients était de 37,5 ans avec un sexe ratio de 1. Le délai moyen d'apparition des signes était de 23 jours. Les réactions immunoallergiques observées étaient 5 cas de toxidermie généralisée, un cas de Dress syndrome, un cas de neutropénie, un cas de pancitopénie et 2 cas de thrombopénie. Le délai moyen de disparition des manifestations immunoallergiques était de 14 jours. Les caractéristiques des 10 patients et les médicaments réintroduits du moins au plus incriminé selon le tableau clinique sont résumés dans le Tableau 1. L'identification de l'antibacillaire responsable était faite par un test de réintroduction en commençant par le médicament le moins incriminé selon les tableaux cliniques. L'imputabilité de la pyrazinamide était retenue dans 5 cas, alors que celle de l'éthambutol, l'izoniaside, la streptomycine, la rifampicine et l'association pyrazinamide + éthambutole + isoniazide était retenue dans 1 cas respectivement . Le protocole de réintroduction est résumé dans le Tableau 2. Tous les patients avaient bien évolué cliniquement et bactériologiquement aprčs l'adoption d'un régime thérapeutique excluant le ou les médicaments incriminés.
Mécanismes des réactions immunoallergiques aux antibacillaires:
Les antituberculeux peuvent induire des réactions d'hypersensibilité de type I ŕ IV, selon la classification de Gell et Coombs [3,4]: type I: anaphylaxie ou encore hypersensibilité immédiate; type II: hypersensibilité cytotoxique; type III: hypersensibilité semi retardée; type IV: hypersensibilité retardée. Les mécanismes en cause sont variés et loin d'ętre parfaitement élucidés. Lorsqu'elles sont authentiquement liées ŕ une allergie, les réactions immédiates (dans l'heure qui suit la derničre prise) ou trčs accélérée, de type urticaire/angioedčme ou choc par exemple sont le plus souvent IgE dépendantes. Quant aux réactions non immédiates, (exemple les exanthčmes maculo-papuleux), elles impliquent une activation des lymphocytes T spécifiques et répondent ŕ plusieurs mécanismes immunologiques [5,6] (Tableau 3).
Les signes cliniques des réactions immunoallergiques aux antibacillaires: Les manifestations cutanées de l'allergie aux antibacillaires sont multiples, allant d'une simple urticaire au décollement cutané, parfois mortel. Des dermatoses sévčres peuvent ętre observées avec les antituberculeux, comme le syndrome de Stevens-Johnson (SSJ) et de Lyell (SL). Bien qu'il soit exceptionnel, ces derniers ont été décrits avec la rifampicine et la streptomycine [7]. Ils surviennent 7 ŕ 21 jours aprčs le début du traitement. Pour Roujeau et Stern le risque est maximal pendant les deux premiers mois [8,9]. Dans notre série le délai moyen des dermatoses sévčres est estimé ŕ 23 jours. Drira et al. [10] ont rapporté un cas de toxidermie ŕ tous les antituberculeux. Dans une autre étude, deux cas de toxidermie généralisée sévčre ont été notés, le premier imputé ŕ la rifampicine [11] et le second ŕ la streptomycine et au pyrazinamide [12]. Dans notre étude on rapporte un cas de Dress syndrome secondaire ŕ 3 anti-bacillaires : isoniazide, pyrazinamide et éthambutol (Figure 1, Figure 2), et cinq cas de toxidermie généralisée secondaire ŕ la streptomycine, ŕ l'éthambutol ,ŕ l'isoniazide et au pyrazinamide (Figure 3). Ces cas sont rares mais graves pouvant mettre en jeu le pronostic vital, d'oů la décision d'un arręt définitif des médicaments incriminés.
Les effets indésirables immunoallergiques hématologiques sont représentés en premier par la thrombopénie qui est un accident rare mais grave qui peut ętre observé avec tous les antituberculeux. L'antibacillaire le plus fréquemment incriminé est la rifampicine, dans une moindre mesure l'isoniazide et de maničre exceptionnelle le pyrazinamide [13,14] La fréquence des neutropénies induites par le traitement antituberculeux est difficile ŕ évaluer. Elle varie de 0,06 % ŕ 2,3 % [15, 16] et est fréquemment associée ŕ une thrombopénie [16]. Dans notre série on a décrit deux cas de thrombopénie et un cas de leucopénie secondaire ŕ la pyrazinamide et deux autre cas de thrombopénie et pancitopénie dues ŕ la rifampicine.
Conduite ŕ tenir devant les réactions immuno-allergiques aux antibacillaires:
Notre conduite dépendait du type de l'allergie, de la sévérité du tableau clinique et du médicament suspecté. La premičre étape du diagnostic d'une allergie aux antibacillaires repose sur un interrogatoire minutieux afin de préciser: Le mode de début; La symptomatologie clinique: voir les personnes en aigu ou avoir des photos des lésions est important; La chronologie des symptômes: contacts antérieurs avec le médicament en cause, délai d'apparition aprčs la derničre prise, effet de l'arręt qui n'est pas toujours concluant...; Les antécédents du patient: notion d'incidents allergiques antérieurs, en présence ou en dehors de toute prise médicamenteuse, pathologies associées, prise médicamenteuse concomitante...; Les signes de gravité dont la présence doit faire suspecter, rechercher et traiter rapidement un choc anaphylactique, un œdčme laryngé, un syndrome de Lyell ou de Stevens-Johnson, une vascularite, ou un syndrome d'hypersensibilité avec atteintes multi-organes ou DRESS. La présence de ces signes de gravité doit faire doser quelques paramčtres biologiques (Tableau 4) et arręter immédiatement le traitement [17].
Devant une forte suspicion clinique et en l'absence de moyen de réalisation des tests cutanés -qui ne sont pas encore validés pour les antibacillaires et aussi vu l'indisponibilité dans notre contexte de leur forme injectable - l'arręt d'un ou de plusieurs médicaments associé ŕ un traitement symptomatique en cas de nécessité (corticoďdes et / antihistaminiques') est préconisée comme premičre étape. Par la suite (et seulement si nécessité absolue du médicament) on tente de réadministrer les antibacillaires ŕ des doses progressives, l'un aprčs l'autre en gardant en dernier le plus suspect de la réaction d'hypersensibilité, c'est le test de réintroduction. Ce test permettra d'identifier le médicament responsable. Alors devant les réactions allergiques graves, chez des patients ayant des formes pauci-bacillaires non étendues, l'arręt définitif du médicament fortement suspecté est conseillé.
Les effets indésirables des antituberculeux sont variables, parfois imprévisibles et potentiellement graves. Notre étude a montré une fréquence significative des complications graves qui restent sous-estimées (25.6% selon notre étude). La survenue d'un effet indésirable évoquant le rôle des antituberculeux pose le problčme de l'identification du produit responsable en absence de validité du bilan allergologique clairement établie pour l'allergie aux antibacillaires
Les atueurs ne déclarent aucun conflit d'intéręts.
Tous les auteurs ont contribués ŕ l'élaboration de ce travail. Tous ont lu et approuvé la version finale du manuscrit.
Tableau 1: caractéristique des patients ayant nécessité l’arręt définitif du médicament incriminé.
Tableau 2: protocole de réintroduction des médicaments dans notre série.
Tableau 3: classification des réactions immunologiques provoquées par les médicaments [adaptée d'aprčs 55,6].
Tableau 4: signes de gravité (cliniques et biologiques) ŕ rechercher rapidement devant toute suspicion d’allergie médicamenteuse
Figure 1: exanthčme maculeux du visage chez un patient qui a prsenté un DRESS syndrome attribué ŕ 3 antibacillaires : isoniazide, pyrazinamide et éthambutol
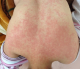
Figure 2: exanthčme diffus du tronc chez un patient qui a prsenté un DRESS syndrome attribué ŕ 3 antibacillaires : isoniazide, pyrazinamide et éthambutol
Figure 3: toxidermie généralisée attribuée ŕ la pyrazinamide
- Imbart-comte L, Demoly P. Les accoutumances médicamenteuses. Revue française d'allergologie et d'immunologie clinique. 2004 ; 44(3): 308-314. PubMed | Google Scholar
- Pur ozyigit LP, Galerac ,Defrance C, Kilicaslan Z , Demoly P. Allergie aux antituberculeux, une solution thérapeutique pragmatique : la désensibilisation au rifater. Revue française d'allergologie. 2011 ; 51(4) : 446-448. PubMed | Google Scholar
- Gruchalla R. Understanding drug allergies. J Allergy Clin Immunol. 2000 june; 105(6Pt2): s634-7. PubMed | Google Scholar
- Fenniche S, Maalej S, Fekih L, Hassene H, Belhabib D, Megdiche ML. Manifestations d'hypersensibilité ŕ la rifampicine. Presse Med. 2003 Jule; 32(25): 1167-9. PubMed | Google Scholar
- Portales-casamar s, Demoly p. Cdrom encyclopédique d'allergologie. Resip. Edition 200. PubMed | Google Scholar
- Pichler WJ. Delayed drug hypersensitivity reactions. Ann Intern Med. 2003; 139(8): 683-93. PubMed | Google Scholar
- Goldin HM, Schweitzer WJ, Bronson DM. Rifampicin and exfoliative dermatitis. Ann Intern Med. 1987; 107(5): 789. PubMed | Google Scholar
- Roujeau JC. Toxic epidermal necrolysis and stevens-johnson syndrome. Rev Prat. 2007; 57(11): 1165-70. PubMed | Google Scholar
- Roujeau JC, Stern RS. Severe adverse cutaneous reactions to drugs. N Engl J Med. 1994; 331(19): 1272-85. PubMed | Google Scholar
- Drira I, Souissi R, Dakhlaoui R, Jeguirim MS, Chebbi ML. Désensibilisation orale aux antituberculeux. Rev Pneumol Clin. 1997; 53(2): 104-6. PubMed | Google Scholar
- Matz T, Borish LC, Routes JM, Rosenwasser LJ. Oral desensitization to rifampicin and ethambutol in mycobacterial disease. Am J Respir Crit Care Med. 1994; 149 (3 Pt 1): 815-7. PubMed | Google Scholar
- Leophonte p, Didier a, carre p, Pouchelon e, Rouquet rm. Modalites thérapeutiques de la tuberculose pulmonaire. Rev Prat. 1990; 40(8): 719-4. PubMed | Google Scholar
- Denis J, Robert A, Johanet C, Homberg JC, Opolon P, Levy VG. Accident immunoallergique ŕ la rifampicine avec coagulation intravasculaire disséminée. Presse Med. 1983; 12(23): 1479-81. PubMed | Google Scholar
- Lee CH, Lee CJ. Thrombocytopenia: a rare but potentially serious side effect of initial daily and interrupted use of rifampicin. Chest. 1989; 96(1): 202-3. PubMed | Google Scholar
- Shishido Y, Nagayama N, Masuda K, Baba M, Tamura A, Nagai H, Akagawa S. Agranulocytosis due to anti-tuberculosis drugs including isoniazid (inh) and rifampicin (rfp) - a case report of four cases and review of the literature. Kekkaku. 2003; 78(11): 683-9. PubMed | Google Scholar
- Nagayama N, Shishido Y, Masuda K, Baba M, Tamura A, Nagai H, Akagawa S. Leukopenia due to anti-tuberculous chemotherapy including rifampicin and isoniazid. Kekkaku. 2004; 79(5): 341-8. PubMed | Google Scholar
- Demoly P, Hillaire-buys D, Raison-peyron N, et al. Comprendre les allergies médicamenteuses. Médecine/Sciences. 2003; 19(3):327-36. PubMed | Google Scholar