Leucémie aigue érythroblastique: ŕ propos de sept observations
Imane Tlamçani, Salma Benjelloun, Ghita Yahyaoui, Moncef Hassani Amrani
Corresponding author: Imane Tlamçani, Laboratoire d’Hématologie, Laboratoire Central d’Analyses Médicales, CHU Hassan II, Fčs, Maroc 
Received: 27 Jan 2014 - Accepted: 12 May 2014 - Published: 18 May 2014
Domain: Clinical medicine
Keywords: Erythroleucémie, leucémie érythroïde pure, frottis sanguin, médullogramme, imunophénotypage
©Imane Tlamçani et al. Pan African Medical Journal (ISSN: 1937-8688). This is an Open Access article distributed under the terms of the Creative Commons Attribution International 4.0 License (https://creativecommons.org/licenses/by/4.0/), which permits unrestricted use, distribution, and reproduction in any medium, provided the original work is properly cited.
Cite this article: Imane Tlamçani et al. Leucémie aigue érythroblastique: ŕ propos de sept observations. Pan African Medical Journal. 2014;18:61. [doi: 10.11604/pamj.2014.18.61.3921]
Available online at: https://www.panafrican-med-journal.com//content/article/18/61/full
Leucémie aigue érythroblastique: ŕ propos de sept observations
Imane Tlamçani1,&, Salma Benjelloun1, Ghita Yahyaoui1, Moncef Hassani Amrani1
1Laboratoire d’Hématologie, Laboratoire Central d’Analyses Médicales, CHU Hassan II, Fčs, Maroc
&Auteur correspondant
Imane Tlamçani, Laboratoire d’Hématologie, Laboratoire Central d’Analyses Médicales, CHU Hassan II, Fčs, Maroc
La leucémie aigue érythroblastique (LAM-M6) est une entité rare, représente 3 ŕ 4% de l'ensemble des leucémies aigues. Il en existe deux types : l'érythroleucémie et la leucémie érythroďde pure. Elle se manifeste le plus souvent par des signes de cytopénie et d'infiltration des tissus extra-hématopoďétiques, elle est plus fréquente chez les adultes que chez les enfants et est de mauvais pronostic. Le but de notre travail est de mettre en évidence les particularités épidémiologiques, diagnostiques et évolutives de cette pathologie rare au sein du CHU HASSAN II de Fčs. Nous rapportons le cas de sept patients diagnostiqués leucémie aigue érythroblastique LAM-M6 au laboratoire d'hématologie du CHU Hassan II de Fčs entre Janvier 2009 et Aout 2013. Le diagnostic de leucémie aigue érythroblastique a été retenu sur un examen cytologique du frottis sanguin et du médullogramme ainsi que l'examen immunophénotypique. Il s'agit de deux adultes et cinq enfants, la plupart ont présenté une altération de l'état général, des signes de cytopénie et un syndrome tumoral. L'étude cytologique du frottis sanguin et du médullogramme ainsi que les résultats de l'immunophénotypage ont conduit au diagnostic de l'érythroleucémie chez six de nos patients et de leucémie érythroďde pure chez un seul patient. L'évolution a été différente pour ces patients. Le pronostic est grave d'oů l'intéręt d'un diagnostic rapide et d'une prise en charge adéquate.
La leucémie aigue érythroblastique est caractérisée par la prolifération d'une population érythrocytaire prédominant sur les autres lignées. On en distingue deux types : -érythroleucémie : définie par la présence dans la moelle osseuse de plus de 50% des précurseurs érythroďdes de l'ensemble des cellules médullaires, et de plus de 20% de myéloblastes de l'ensemble des cellules médullaires non érythrocytaires - Leucémie érythroďde pure : elle présente une prolifération néoplasique faite de plus de 80% de cellules érythrocytaires sans présence évidente du contingent myéloblastique.
L'érythroleucémie est une maladie rare, elle représente 3 ŕ 4% des cas de leucémies aigues myéloďdes et est prédominante chez le sujet âgé. Quant ŕ la leucémie érythroďde pure, elle est exceptionnelle et peut concerner tous les âges y compris les enfants [1]. Nous essayons ŕ travers ce travail de mettre le point sur les différentes particularités épidémiologiques, diagnostiques et évolutives de cette pathologie rare au niveau du CHU HASSAN II de Fčs et dont le diagnostic a été posé au service d'hématologie du laboratoire central d'analyses médicales.
Dans cette étude, nous rapportons le cas de sept patients diagnostiqués LAM-M6 au service d'hématologie du CHU Hassan II de Fčs entre Janvier 2009 et Aout 2013. Il s'agit de deux adultes de sexe masculin, âgés de 62 et 80ans respectivement, et de cinq enfants d'âges différents allant de 2mois ŕ 8ans. Les patients adultes étaient hospitalisés au service de médecine interne, et les enfants au service de pédiatrie. Nous avons réalisé, pour tous les patients, des frottis sanguins qu'on a colorés ŕ la coloration de May-Grünwald-Giemsa, et des frottis médullaires qu'on a colorés également ŕ la coloration de May-Grünwald-Giemsa et ŕ la myéloperoxydase. Un examen immunophénotypique sanguin et/ou médullaire a été effectué dans tous les cas.
La majorité des patients est issue d'un niveau socio-économique bas et le motif de consultation majeur est l'asthénie associée le plus souvent ŕ un syndrome anémique. L'incidence de la leucémie aigue érythroblastique par rapport aux autres leucémies aigues diagnostiquées au laboratoire d'hématologie du CHU HASSAN II de Fčs est de 5%. L'âge moyen de nos patients est de 22,4 ans, et le sexe ratio est H/F=6 (Tableau 1). Tous les patients présentent une fičvre et une altération d'état général au moment du diagnostic, 85% d'entre eux ont un syndrome tumoral.
Tous les patients présentent une anémie profonde associée ŕ une thrombopénie. Trois des sept patients (enfants) ont un purpura pétéchial ŕ l'admission. L'hyperleucocytose est présente chez trois patients et la leucopénie chez un seul. La fičvre est retrouvée chez tous les patients mais aucun foyer infectieux n'a été mis en évidence (Tableau 1). Le frottis sanguin montre la présence de blastes périphériques dans 71% des cas (Tableau 2).
Dans cette étude, tous les médullogrammes de nos patients répondent aux critčres morphologiques établis par la classification FAB (Franco-Américano-Britannique) pour le diagnostic de LAM-M6. Chez six de nos patients, la moelle est hypercellulaire avec un taux de myéloblastes supérieur ŕ 20% par rapport ŕ tous les éléments non érythroblastiques et une hyperplasie érythroblastique estimée ŕ plus de 50% ; avec des signes de dysérythropoďčse ce qui a fait évoquer le diagnostic d'érythroleucémie. Un seul patient a une hyperplasie érythroblastique chiffrée ŕ 82% avec 14% de myéloblastes sur les éléments non érythroblastiques, le diagnostic de leucémie érythroďde pure est évoqué (Figure 1, Figure 2, Tableau 2).
Une coloration cytochimique de la myéloperoxydase est réalisée pour tous les médullogrammes et est positive dans tous les cas (Figure 3). L'immunophénotypage sanguin est réalisé pour tous les patients et est positif pour MPO, CD13, CD33 et la Glycophotine A. Quatre de nos patients ont bénéficié d'une étude cytogénétique. Le bilan biochimique a montré un syndrome de lyse tumorale dans tous les cas.
Deux enfants sont décédés au décours du diagnostic. Un patient adulte a refusé le traitement et est décédé aprčs quatre mois suite aux complications. Les autres patients ont été mis sous chimiothérapie, deux d'entre eux sont décédés au cours du traitement. Les deux enfants vivants sont toujours sous traitement et évoluent bien sous chimiothérapie.
La leucémie aigue érythroblastique est une entité trčs rare. Une anémie importante en est le signe habituel ; elle donne lieu ŕ une asthénie profonde. Un syndrome infectieux et/ou hémorragique peuvent ętre révélateurs. Une hépatomégalie et/ou splénomégalie peuvent ętre présents [1,2].
Dans notre série, six de nos patients sont de sexe masculin, la moyenne d'âge est de 22,4 ans avec des extręmes d'âge de 2 mois et de 80 ans. Cinq de nos patients sont de bas âge y compris un nourrisson de deux mois. La particularité de notre étude réside dans la fréquence élevée des formes pédiatriques de cette pathologie rare contrairement aux cas rapportés dans la littérature oů la forme adulte est la plus fréquente [1,2].
Tous les patients présentent des signes en rapport avec la cytopénie et la présence d'un syndrome tumoral associé. Le diagnostic biologique est posé devant les résultats de la numération formule sanguine, le frottis sanguin, le médullogramme et l'immunophénotypage.
Tous les hémogrammes ont montré la présence d'une bicytopénie (anémie et thrombopénie), trois d'entre eux présentent par ailleurs un purpura pétéchial ŕ l'admission. Trois des sept patients présentent une hyperleucocytose et un seul présente une leucopénie; ce qui rejoint la plupart des cas décrits dans d'autres études [1,2]. Le frottis sanguin montre la présence de blastes circulants dans 71% des cas. Dans la littérature, ce taux varie entre 37,4% et 85,2% [1,3].
Au total, la présentation clinique et hématologique de la leucémie aigue érythroblastique est semblable aux tableaux des autres leucémies aigues, cependant la principale différence se situe au niveau de la moelle osseuse et de l'immunophénotypage.
Dans l'érythroleucémie, tous les stades de maturation des précurseurs érythroďdes peuvent ętre présents avec prédominance des formes immatures. Les précurseurs érythroďdes sont dysplasiques avec éventuellement des formes mégaloblastiques et/ou multinuléées. Le cytoplasme des cellules immatures contient souvent des vacuoles mal limitées qui peuvent fusionner. Les myéloblastes sont de taille moyenne, le cytoplasme contient souvent quelques granulations avec parfois des corps d'Auer. La coloration cytochimique de la myéloperoxydase peut ętre positive dans les myéloblastes [2,3].
L'érythroleucémie doit ętre distinguée des anémies réfractaires avec excčs de blastes (AREB) et leucémies aigues myéloďdes (LAM) avec maturation et un taux élevé de précurseurs érythroďdes. Un comptage de toutes les cellules médullaires doit ętre effectué. Si le taux des précurseurs érythroďdes est supérieur ŕ 50% par rapport ŕ toutes les cellules médullaires, un comptage des cellules non érythroďdes doit ętre calculé. Si les blastes sont supérieurs ŕ 20% par rapport aux cellules non érythroďdes, le diagnostic est celui de l'érythroleucémie (érythroďde/myéloďde). Si le taux de blastes est inférieur ŕ 20%, le diagnostic est celui de l'AREB [4]. Le diagnostic différentiel inclut également la leucémie aigue myéloďde avec dysplasie multilignée si la dysplasie intéresse plus de 50% des lignées myéloďde ou mégacaryocytaire.
Les érythroblastes ne sont généralement pas associés ŕ des marqueurs myéloďdes et sont négatifs aux anti-MPO, ils réagissent avec des anticorps de la glycophorine A et de l'hémoglobine A. Les myéloblastes expriment une variété d'antigčnes myéloďdes associés, y compris : CD13, CD33, CD117 et MPO avec ou sans expression des marqueurs des précurseurs cellulaires, par exemple : CD34 et HLA-DR classe II qui sont des déterminants similaires des blastes d'autres types de LAM [3-5]. Tous les aspects cytologiques décrits dans la littérature sont retrouvés dans notre étude en plus des signes de dysplasie touchant essentiellement la lignée érythrocytaire (<50% de la lignée) et moins fréquemment les lignées mégacaryocytaire et granuleuse [5-7]. La coloration cytochimique de la myéloperoxydase a été positive dans tous les cas ainsi que la présence de marqueurs myéloďdes et érythroblastiques lors de l'immunophénotypage.
Quant ŕ la leucémie érythroďde pure, elle est caractérisée par la présence d'érythroblastes de taille moyenne ŕ grande, souvent ŕ noyau arrondi et ŕ chromatine fine, avec des formes mono et multinucléées. Le cytoplasme est basophile, agranulaire et contenant parfois quelques vacuoles mal limitées [8, 9]. Le diagnostic différentiel de la leucémie érythroďde pure comprend l'anémie mégaloblastique due ŕ une carence en vitamine B12 ou en acide folique [8-10]. Les patients présentant une carence en vitamine B12 et/ou en acide folique répondent au traitement vitaminique, et la dysplasie n'est généralement pas aussi marquée que dans la leucémie érythroďde pure. La segmentation prématurée des précurseurs neutrophiles est une preuve supplémentaire de la carence en vitamine B12 ou en folates [9,10]. Les formes les plus différenciées peuvent ętre détectées par l'expression de la glycophorine A et l'hémoglobine A, et l'absence de marqueurs myéloďdes. Les blastes sont souvent négatifs aux anticorps monoclonaux du systčme HLA-DR classe II et les CD34.
Les formes les plus immatures sont généralement négatives pour la glycophorine A ou faiblement exprimés dans une minorité de blastes. Autres marqueurs tels que l'anhydrase 1 carbonique, CD36 sont habituellement positifs pour les progéniteurs érythroďdes ŕ des stades précoces de leur différenciation. Le CD36 n'est pas spécifique pour les érythroblastes et peut ętre exprimé par les monocytes et les mégacaryocytes [11]. Les antigčnes associés des mégacaryocytes (CD41 et CD61) sont généralement négatifs mais peuvent ętre partiellement exprimés dans certains cas [12]. Dans notre série, un seul patient est diagnostiqué leucémie érythroďde pure (enfant de trois ans et demi). Au médullogramme, on retrouve une moelle hypercellulaire avec hyperplasie érythroblastique, tous les stades de maturation étant représentés. Le contingent myéloblastique est estimé ŕ 14% compté sur la population non érythrocytaire, fait de blastes de taille moyenne, ŕ noyau arrondi, chromatine fine et souvent nucléolée, cytoplasme peu étendu et basophile contenant parfois des corps d'Auer. La coloration cytochimique ŕ la myéperoxydase est discrčtement positive. Quant ŕ la lignée érythroblastique, elle est estimée ŕ 82% faite le plus souvent de mégaloblastes ŕ noyau arrondi et ŕ chromatine fine. L'étude immunophénotypique est positive également pour la Glycophorine A. Le dosage de la vitamine B12 et de l'acide folique est normal ce qui a conclu au diagnostic de LAM-M6 en tenant compte du contexte clinique. Cuneo et al a effectué une étude d'une série de 26 patients avec leucémie aigue érythroblastique et a établi leurs caractéristiques cliniques, morphologiques et cytogénétiques. L'analyse des données de cette étude a montré que lorsque la LAM-M6 est définie par des critčres morphologiques, on peut distinguer deux sous groupes [5]: -les patients du premier groupe ont tendance ŕ ętre plus âgés, avec des anomalies cytogénétiques complexes en particulier des chromosomes 5 et/ou 7, ont un pronostic défavorable. La durée de rémission est courte en utilisant la chimiothérapie conventionnelle. Il est concevable que l'accumulation progressive de l'ensemble de ces altérations génétiques soit importante pour la progression de la maladie de LAM-M6. -Ceux du deuxičme groupe ne présentent pas d'anomalies cytogénétiques décelables ou caryotype normal, ont un pronostic plus favorable lorsqu'ils sont traités par une chimiothérapie conventionnelle [5].
Nos patients ayant bénéficié d'une étude cytogénétique ne présentent pas d'aberrations chromosomiques particuličres. Le diagnostic a été retenu en se basant sur l'aspect morphologique et immunophénotypique. Dans notre série, l'évolution des patients a été différente ; cinq sont décédés au décours du diagnostic et du traitement, et deux évoluent bien sous chimiothérapie conventionnelle. Comparativement ŕ d'autres séries, l'évolution de la leucémie aigue érythroblastique est agressive avec une médiane de survie courte [8,9].
Il n'existe pas d'anomalies cytogénétiques spécifiques décrites dans ce type de leucémie. Des caryotypes complexes avec des anomalies de structure sont communs avec atteinte fréquente des chromosomes 5 et 7. Les patients avec des caryotypes complexes ou des anomalies des chromosomes 5 et/ou 7 ont un taux plus élevé de rechute que ceux qui ont des caryotypes normaux. Lors de l'induction de la rémission de la maladie, la durée est plus courte par rapport aux autres sous-types des LAM, c'est un signe de mauvais pronostic. Les patients ayant bénéficié d'une greffe de moelle osseuse ont un taux de rechute moins élevé. La greffe de moelle osseuse peut ętre discutée lors de la premičre rémission complčte en particulier chez les patients ŕ caryotype complexe avec anomalies chromosomiques [4, 5].
Les auteurs ne déclarent aucun conflit d'intéręts.
Tous les auteurs ont contribué ŕ la prise en charge des patients et ŕ la rédaction du manuscrit. Tous ont lu et approuvé la version finale du manuscrit.
Tableau 1: Différentes anomalies retrouvées dans les hémogrammes chez tous les patients de notre série
Tableau 2: Différentes anomalies cytologiques retrouvées au niveau des frottis sanguins et myélogrammes chez tous les patients
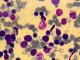
Figure 1: Frottis médullaire
montrant une moelle hypercellulaire avec présence de nombreux éléments de la
lignée éryhtrocytaire avec différents stades de maturation (objectif x 10 et
20
respectivement)
Figure 2: Moelle osseuse
hypercellulaire infiltrée par un contingent érythroblastique dépassant 50% de
l’ensemble des cellules médullaires avec des signes de dysérythropoďčse (objectif
x100)
Figure 3: Présence de
myéloblastes discrčtement positifs ŕ la coloration cytochimique de la myéloperoxydase
- Killick S, Matutes E. Acute Erythroid leukaemias. Atlas Genet Cytogenet Oncol Haematol. July 2002; URL http://AtlasGeneticsOncology.org/Anomalies/M6ANLLID1215.html.
- Jaffe ES, Harris NL, Diebold J, Müller-Hermelink HK. World Health Organization classification of neoplastic diseases of the hematopoietic and lymphoid tissues: a progress report, Pathol Patterns, 1998. Am J Clin Pathol 1999; 111 (suppl.): S8-S12. PubMed | Google Scholar
- Killick S, Matutes E, Powles RL, Min T, Treleaven JG, Rege KP, Atra A, Catovsky D. La leuc émie aigue érythroďde (M6): résultat de la transplantation de moelle osseuse. Leukemia and Lymphoma. 1999; 35(1-2): 99-107. PubMed | Google Scholar
- Olopade OI, Thangavelu M, Larson RA, Mick R, Kowal-Vern A, at al. Clinical, morphologic, and cytogenetic characteristics of 26 patients with acute erythroblastic leukemia. Blood. 1992 Dec; 80(11):2873-82. PubMed | Google Scholar
- Cuneo A, Van Orshoven A, Michaux JL, Boogaerts M, Louwagie A, Doyen C, Dal Cin P, Fagioli F, Castoldi G, Van den Berghe H. Morphologic, immunologic and cytogenetic studies in erythroleukaemia: evidence for multilineage involvement and identification of two distinct cytogenetic-clinicopathological types. Br J Haematol. 1990 Jul; 75(3):346-54. PubMed | Google Scholar
- Jogai S1, Varma N, Garewal G, Das R, Varma S. Acute erythroleukemia (AML-M6)-a study of clinicohematological, morphological and dysplastic features in 10 cases. Indian J Cancer. 2001 Jun-Dec; 38(2-4):143-8. PubMed | Google Scholar
- Batra VV, Karan AS, Saxena R. Erythroleukemia: a clinco-hematological review of four cases. Indian Pediatr. 2004 Jun; 41(6):587-90. PubMed | Google Scholar
- Rodrigues CA, Chaufaille ML, Pelloso LA, Ghaname FS, et al. Acute myeloid leukemia in elderly patients: experience of a single center. Braz J Med Biol Res. 2003 Jun; 36(6):703-8. PubMed | Google Scholar
- Pulsoni A, Pagano L, LatagliataR, Casini M, Cerri A, Crugnola M, De Paoli L et al. Survival of elderly with acute myeloid leukemia. Haematologica. 2004 Mar; 89(3):296-302. PubMed | Google Scholar
- Bennett JM, Catovsky D, Daniel MT, Flandrin G, Galton DAG, et al. Proposals for the classification of the acute leukaemias: French-American-British Cooperative Group. Br J Haematol. 1976 Aug;33(4): 451-58. PubMed | Google Scholar
- Bennett JM, Catovsky D, Daniel MT, Flandrin G, Galton DAG, Gralnick HR, Sultan C. Proposed revised criteria for the classification of acute myeloid leukemia: a report of the French-American-British Cooperative Group. Ann Intern Med. 1985 Oct;103(4): 626-29. PubMed | Google Scholar
- Nakamura H. Cytogenetic heterogeneity in erythroleukemia defined as M6 by the French-American-British (FAB) Cooperative Group criteria. Leukemia. 1989 Apr; 3(4):305-9. PubMed | Google Scholar