Necrolyse épidermique toxique induite par le phenobarbital chez un enfant Rwandais: ŕ propos d’un cas
Célestin Kaputu-Kalala-Malu, Olga Ntumba-Tshitenge, Jean-Paul Misson
Corresponding author: Célestin Kaputu-Kalala-Malu, Service of Child Neurology, Department of Neurology, Kinshasa School of Medicine, University of Kinshasa, Democratic Republic of Congo 
Received: 16 Sep 2013 - Accepted: 03 Dec 2013 - Published: 14 Mar 2014
Domain: Clinical medicine
Keywords: Syndrome de Lyell, phénobarbital, enfant, Afrique
©Célestin Kaputu-Kalala-Malu et al. Pan African Medical Journal (ISSN: 1937-8688). This is an Open Access article distributed under the terms of the Creative Commons Attribution International 4.0 License (https://creativecommons.org/licenses/by/4.0/), which permits unrestricted use, distribution, and reproduction in any medium, provided the original work is properly cited.
Cite this article: Célestin Kaputu-Kalala-Malu et al. Necrolyse épidermique toxique induite par le phenobarbital chez un enfant Rwandais: ŕ propos d’un cas. Pan African Medical Journal. 2014;17:202. [doi: 10.11604/pamj.2014.17.202.3385]
Available online at: https://www.panafrican-med-journal.com//content/article/17/202/full
Original article 
Necrolyse épidermique toxique induite par le phenobarbital chez un enfant Rwandais: ŕ propos d’un cas
Nécrolyse épidermique toxique induite par le phénobarbital chez un enfant Rwandais: ŕ propos d'un cas
Célestin Kaputu-Kalala-Malu1,&, Olga Ntumba-Tshitenge2, Jean-Paul Misson3
1Service of Child Neurology, Department of Neurology, Kinshasa School of Medicine, University of Kinshasa, Democratic Republic of Congo, 2Department of pediatrics, Butare University Teaching Hospital, National University of Rwanda, Rwanda, 3Service of Pediatrics and Child Neurology, CHR Citadelle Hospital and CHU University Hospital, University of Ličge, Belgium
&Auteur correspondant
Célestin Kaputu-Kalala-Malu, Service of Child Neurology, Department of Neurology, Kinshasa School of Medicine, University of Kinshasa, Democratic Republic of Congo
Le syndrome de Lyell ou la nécrolyse épidermique toxique (TEN) est une des rares complications majeures du traitement par phénobarbital. Sa prise en charge n'est pas encore codifiée. Il requiert une intervention urgente, lourde et adaptée ŕ chaque patient afin d'en réduire la mortalité. Nous décrivons un cas du syndrome de Lyell survenu une dizaine de jours aprčs initiation du traitement antiépileptique par phénobarbital chez un enfant rwandais de deux ans. La complexité des lésions cutanéomuqueuses et leurs répercussions sur le plan général soulignent l'importance d'une prescription responsable et justifiée des médicaments antiépileptiques.
Le phénobarbital est sans aucun doute la médication antiépileptique la plus ancienne et reste également trčs souvent prescrit chez le jeune enfant dans cette indication [1]. A ce titre il est repris dans la liste des médicaments essentiels de l'Organisation Mondiale de la Santé de 2013 [2].Malgré son innocuité apparente, il peut induire des effets secondaires allant du plus bénin au plus grave et mortel ŕ l'instar de nécrolyse épidermique toxique (TEN) connue sous le nom de syndrome de Lyell [3]. La TEN est considérée comme une «allergie» médicamenteuse caractérisée par la destruction brutale de la couche superficielle de la peau (épiderme) et des muqueuses (épithélium). On utilise le nom de syndrome de Lyell pour les formes les plus étendues - plus de 30% de surface corporelle - et celui de syndrome de Stevens-Johnson (SJS) pour les formes limitées de nécrolyse épidermique qui peuvent le rester ou progresser vers un syndrome de Lyell [4] Son incidence a été évaluée ŕ environ 1 cas par million d'habitants par an.En Europe, l'incidence conjointe de la TEN et du SJS est de 2 cas par million d'habitants par an [5]. Sa prise en charge, généralement symptomatique et lourde, est indispensable en urgence. Toutefois, le pronostic reste grave, 20 ŕ 25 % de mortalité et prčs de 50 % de séquelles, en particulier oculaires, chez les survivants [6]. Ŕ notre connaissance, aucun cas de syndrome de Lyell n'a encore été publié en Afrique Centrale.
Un enfant de sexe masculin, âgé de 2 ans et demi, pesant 13 kilogrammes, a été admis, via le service d'urgence pédiatrique, au Centre Hospitalier Universitaire de Butare / Rwanda pour une prise en charge des lésions cutanéomuqueuses disséminées évoluant depuis 7 jours. Les antécédents personnels et familiaux n'étaient pas contributifs en dehors de la survenue des crises épileptiques tonicocloniques généralisées pour lesquelles les parents avaient consulté dans un hôpital de district. Une thérapie anticomitiale faite de phénobarbital ŕ la dose de 50 mg par jour (soit 3,8 mg/kg/dose) a été débutée 19 jours plutôt. L'évolution a été marquée, 12 jours plus tard, par l'apparition de la fičvre (dont l'intensité n'était pas documentée) et d'une éruption érythémateuse étendue. Cette phase a été rapidement suivie par l'apparition des lésions cutanéomuqueuses bulleuses disséminées pour lesquelles l'enfant a été référé au Centre Hospitalier Universitaire de Butare pour meilleure prise en charge.
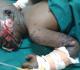
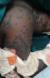
A l'examen physique, l'état général était altéré par la fičvre mesurée ŕ 38,5°C. L'examen dermatologique a révélé des lésions érosives d'allure nécrotique intéressant les muqueuses oculaires et buccales responsables des troubles de vision et d'alimentation. Les lésions cutanées, quant ŕ elles, prédominaient ŕ la tęte, au visage, au cou, aux membres supérieurs, ŕ la ceinture pelvienne ainsi qu'aux membres inférieurs. Elles consistaient en des plages des bulles ŕ toit nécrotique d'allure confluant séparées par des plages de nécrose épidermique réalisant un décollement en « linge mouillé » typique avec le signe de Nikolsky (Figure 1, Figure 2 ). La surface corporelle atteinte a été évaluée ŕ 35%. Sur la base des éléments objectifs et anamnestiques, le diagnostic du syndrome de Lyell induit par le phénobarbital a été évoqué. Le score prédictif du pronostic (SCROTEN) était estimé favorable car évalué ŕ 2/7 [7]. La biopsie cutanée pour un examen anatomopathologique n'a pas pu ętre réalisée pour des raisons logistiques.
Prise en charge et évolution
D'emblée l'enfant a été admis en soins intensifs dans le but de contrôler de maničre rigoureuse les paramčtres hémodynamiques et de prévenir les désordres hydroélectrolytiques pouvant survenir ŕ cause de la difficulté d'alimentation et des pertes cutanées. Les lésions de muqueuses buccales ont été prises en charge par un tamponnage quotidien au sérum physiologique et l'application du gel oral DaktarinR(Miconazole). La tétracycline ophtalmique suivie d'application des larmes artificielles pour sécheresse oculaire ont constitué l'essentiel des soins oculaires.
La prise en charge des lésions cutanées a consisté en la mise du patient dans une chambre d'isolement pour éviter les surinfections. Les lésions cutanées ont bénéficié de quelques séances de débridements en salle d'opération sous anesthésie générale (KétamineR) et des pansements non adhésifs. L'application de la FLAMAZINERcrčme (Sulfadiazine d´argent ŕ 1%) et de la crčme FUCIDINER (acide Fusidique ŕ 2%) a été effectuée suivant l'état des lésions et les recommandations des fabricants.
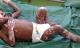
Le paracétamol et le tramadolR ont été utilisés dans la gestion de la douleur. L'évolution a été marquée, dčs le quatričme jour d'hospitalisation par une hyperthermie variant entre 38 °C et 39,7° C malgré la négativité des investigations paracliniques dont 2 hémocultures, 2 analyses cytobactériologique des urines et 2 gouttes épaisses ŕ la recherche de trophozoďtes. Outre les antibiotiques qui avaient été administrés de maničre empiriques (Ampicilline + gentamycine puis céfotaxime et pour finir, amoxilline+ acide clavulanique), cette hyperthermie qui a duré 20 jours a été prise en charge par un enveloppement humide et le paracétamol en alternance avec l'ibuprofčne. La cicatrisation avec la régénération de l'épiderme a débuté vers le 14čme jour suivant l'admission du malade laissant les cicatrices hypochromiques (Figure 3, au 25čme jour d'hospitalisation). Les lésions muqueuses ont été les derničres ŕ cicatriser mais le patient ŕ continuer de présenter, avant sa sortie, une sécheresse oculaire malgré l'application des larmes artificielles. Les contrôles des fonctions rénales et hépatiques étaient normaux au début et ŕ la fin du traitement. L'acide valproďque a été proposé en remplacement du phénobarbital.
Des études d'observation cas-témoins ont établi que la cause la plus fréquente des syndromes de Lyell et de Stevens-Johnson, est une « allergie » médicamenteuse, bien établie dans environ 60 % des cas, plausible dans environ 30 %. Plusieurs médicaments ont été impliqués, au moins une fois, dans la survenue de cette « allergie » mais, moins de dix rendent compte d'environ la moitié des cas en Europe. Il s'agit de la carbamazépine, la lamotrigine, le phénobarbital, la phénytoďne, l'allopurinol, la névirapine, les sulfamides anti-infectieux et les antiinflammatoires non stéroďdiens dérivés de l'oxicam. Parfois, aucun médicament suspect n'est identifié, aucune exposition médicamenteuse n'est retrouvée. Quelques-uns de ces cas d'apparence idiopathique ont été expliqués par des infections, en particulier des pneumopathies atypiques ŕ Mycoplasmapneumonić [5, 6]. Le mécanisme conduisant ŕ la mort par apoptose brutale et disséminée des cellules de l'épithélium de la peau et des muqueuses demeure non élucidé. Un phénomčne de cytotoxicité lymphocytaire contre des cellules épidermiques reconnues comme étrangčres aprčs fixation du médicament responsables de ces réactions sur certaines molécules HLA de classe I est évoqué. Les médiateurs chimiques qui semblent ętre impliqués dans l'amplification violente et diffuse de l'apoptose ne sont pas encore clairement identifiés [8- 10]. Les hôpitaux situés en Afrique Subsaharien ont un triple défi ŕ relever devant cet "effet secondaire" majeur lié ŕ la prise du phénobarbital qui est, sans aucun doute, l'antiépileptique le plus consommé grâce ŕ son prix abordable et compte tenu de l'incidence et de la prévalence élevées de l'épilepsie dans cette partie du monde.
Le premier défi est d'ordre diagnostic. La rareté de ces syndromes et le manque d'un personnel qualifié dans le maniement des antiépileptiques ainsi qu'en la détection rapide des effets secondaires peuvent faire retarder le diagnostic et la mise en branle d'une prise en charge adaptée comme c'est dans le cas que nous venons de décrire.
Le deuxičme défi est thérapeutique. La prise en charge des syndromes de Lyell et de Stevens-Johnson n'est pas codifiée, elle requiert parfois une multidisciplinarité (neurologue ou pédiatre, dermatologue, chirurgien esthétique, anesthésiste, stomatologue, dentiste, anatomopathologiste, microbiologiste ). Qui n'est pas facile ŕ mettre en place. Ŕ part les ressources humaines, les ressources matérielles utiles pour diagnostiquer les complications ŕ temps (troubles électrolytiques, troubles des gaz sanguins ) afin de réajuster le traitement en cours ne sont pas toujours disponibles dans les institutions hospitaličres les plus fréquentées. C'est dans cet ordre d'idée que nous n'avons pas pu savoir si l'hyperthermie présentée par le patient était seulement dű aux perturbations de la thermorégulation rencontrée dans la TEN [6] ou ŕ une surinfection par un germe nosocomial qui n'a pas pu ętre isolé.
Enfin, il y a le défi d'ordre prévisionnel. Il sied de rappeler que l' « éducation ŕ la prise des antiépileptique» fait partie intégrante de la thérapeutique antiépileptique. Ceux qui sont appelés ŕ prescrire les antiépileptiques, notamment le phénobarbital, doivent informer les nouveaux patients sur le risque réel des effets secondaires graves. Ce risque est particuličrement élevé durant les deux premiers mois suivant l'initiation du traitement par phénobarbital [11]. Un accent devrait ętre mis sur l'arręt immédiat de la molécule récemment prescrite et la consultation sans délai ŕ la moindre apparition d'une lésion cutanée ou muqueuse non autrement expliquée.
L'administration des antiépileptiques et particuličrement du phénobarbital doit ętre faite suivant les indications rigoureuses. La reconnaissance rapide d'une lésion cutanée ou muqueuse non autrement expliquée dans les jours ou semaines suivant l'initiation du phénobarbital doit ętre suivie de son arręt immédiat et d'une consultation dans un hôpital mieux équipé afin de réduire la morbidité et la mortalité chez les patients.
Les auteurs ne déclarent aucun conflit d'intéręts
Célestin Kaputu-Kalala-Malu et Olga Ntumba-Tshitenge ont contribué de maničre égale dans la recherche et la rédaction de ce cas clinique en qualité de premier auteur. Jean-Paul Misson a supervisé la rédaction et a corrigé la version finale de l'article.
Les auteurs remercient le personnel médical ayant contribué, de maničre directe ou indirecte, ŕ la prise en charge médical et chirurgical de ce patient.
Figure 1: Lésions érosives d’allure nécrotique au niveau de la muqueuse buccale. Lésions cutanées associant bulles flasques et nécrose épidermique laissant le derme ŕ nu au niveau du visage, du cou et des membres supérieurs
Figure 2: Lésions cutanées associant bulles flasques et nécrose épidermique réalisant un décollement en "linge mouillé" typique au niveau de la ceinture pelvienne et des cuisses
Figure 3: Lésions cutanéomuqueuses en voie de cicatrisation. Au 25čme jour d’admission
- Kwan P, Brodie MJ. Phenobarbital for the treatment of epilepsy in the 21st century: a critical review. Epilepsia. 2004; 45 (9): 1141-9114. PubMed | Google Scholar
- WHO Model List of essential medicines (revised April 2013). http://www.who.int/medicines/publications/essentialmedicines/18th_EML_Final_web_8Jul13.pdf.Accessed 16 September 2013.
- Mockenhaupt M, Messenheimer J, Tennis P, Schlingmann J. Risk of Stevens-Johnson syndrome and toxic epidermal necrolysis in new users of antiepileptics. Neurology. 2005;64(7):1134-1138. PubMed | Google Scholar
- Bastuji-Garin S, Rzany B, Stern RS, et al. Clinical classification of cases of toxic epidermal necrolysis, Stevens-Johnson syndrome, and erythema multiforme. Arch Dermatol. 1993;129(1): 92-96. PubMed | Google Scholar
- Roujeau JC, Kelly JP, Naldi L, Rzany B, Stern RS, et al. Medication use and the risk of Stevens-Johnson syndrome or toxic epidermal necrolysis. N Engl J Med. 1995; 333:1600-16007 DOI: 10 1056/NEJM199512143332404. PubMed | Google Scholar
- Roujeau JC. Syndromes de Lyell et de Stevens-Johnson. https://www.orpha.net/data/patho/Pro/fr/LyellStevensJohnson-FRfrPro12597.pdf.Accessed 16 September 2013. PubMed | Google Scholar
- Bastuji-Garin S, Fouchard N, Bertocchi M, Roujeau JC, et al. A severity-of-illness score for toxic epidermal necrolysis. J Invest Dermatol. 2000; 115(2):149-153. PubMed | Google Scholar
- Nassif A, Bensussan A, Boumsell L, Deniaud A, Moslehi H, Wolkenstein P, Bagot M, Roujeau JC. Toxic epidermal necrolysis: effector cells are drug-specific cytotoxic T cells. J Allergy ClinImmunol. 2004; 114(5):1209-1215. PubMed | Google Scholar
- Nassif A, Moslehi H, Le Gouvello S, Bagot M, Lyonnet L, Michel L, Boumsell L, Bensussan A, Roujeau JC. Evaluation of the potential role of cytokines in toxic epidermal necrolysis. J Invest Dermatol. 2004;123(5): 850-855. PubMed | Google Scholar
- Viard I, Wehrli P, Bullani R, Schneider P, Holler N, et al. Autoimmune diseases of the skin, pathogenesis, diagnosis , management. Science. 1998; 282:490-493. PubMed | Google Scholar
- Roujeau JC, Stern RS. Severe adverse cutaneous reactions to drugs. N Engl J Med. 1994; 331(19):1272-1285. PubMed | Google Scholar