Pseudo-Meigs syndrome: ŕ propos d’un cas
Benjelloun Hanane, Morad Sanaa, Zaghba Nahid, Bakhatar Abdelaziz, Yassine Najiba, Bahlaoui Abdelkrim
Corresponding author: Sanaa Morad, Service des Maladies Respiratoires, Centre hospitalier Ibn Rochd, Casablanca, Maroc 
Received: 18 Jan 2014 - Accepted: 21 Jan 2014 - Published: 10 Mar 2014
Domain: Clinical medicine
Keywords: Pseudo-Meigs syndrome, cancer, ovaire, épanchements, CA 125
©Benjelloun Hanane et al. Pan African Medical Journal (ISSN: 1937-8688). This is an Open Access article distributed under the terms of the Creative Commons Attribution International 4.0 License (https://creativecommons.org/licenses/by/4.0/), which permits unrestricted use, distribution, and reproduction in any medium, provided the original work is properly cited.
Cite this article: Benjelloun Hanane et al. Pseudo-Meigs syndrome: ŕ propos d’un cas. Pan African Medical Journal. 2014;17:184. [doi: 10.11604/pamj.2014.17.184.3875]
Available online at: https://www.panafrican-med-journal.com//content/article/17/184/full
Pseudo-Meigs syndrome : ŕ propos d’un cas
Benjelloun Hanane1, Morad Sanaa1,&, Zaghba Nahid1, Bakhatar Abdelaziz1, Yassine Najiba1, Bahlaoui Abdelkrim1
1Service des Maladies Respiratoires, Centre hospitalier Ibn Rochd, Casablanca, Maroc
&Auteur correspondant
Sanaa MORAD, Service des Maladies Respiratoires, Centre hospitalier Ibn Rochd, Casablanca, Maroc
Introduction: Le pseudo-Meigs syndrome comprend une tumeur pelvienne bénigne (en dehors des fibrothécomes ovariens) ou maligne associée ŕ des épanchements, pleural et ou péritonéal, qui disparaissent aprčs l'exérčse tumorale. Nous rapportons l'observation d'une patiente âgée de 47 ans, qui présentait une pleurésie droite associée ŕ une ascite et une tumeur ovarienne maligne. L'évolution aprčs l'exérčse chirurgicale de la masse tumorale męme en l'absence d'une chimiothérapie montrait une disparition des épanchements. Le pseudo-Meigs syndrome est rare. Il nécessite des biopsies pleurales et péritonéales négatives, et la disparition des épanchements aprčs l'exérčse chirurgicale de la tumeur, avant toute chimiothérapie. Une telle distinction est importante aussi bien sur le plan thérapeutique que pronostique.
Le pseudo-Meigs syndrome est une triade comportant une tumeur pelvienne maligne ou bénigne (en dehors des fibro-thécomes ovariens) associée ŕ des épanchements, pleural et péritonéal, qui disparaissent aprčs l'exérčse tumorale [1]. Attribuer ces épanchements pleural et péritonéal, au cours d'un cancer de l'ovaire, ŕ ce syndrome est une situation exceptionnelle qui nécessite des preuves histologiques et surtout évolutives. Nous rapportons un cas au cours d'un cystadénocarcinome ovarien de bonne évolution aprčs l'exérčse chirurgicale et avant de démarrer la chimiothérapie.
Une patiente âgée de 47 ans, en périménopause, sans antécédents pathologiques particuliers. Elle consultait pour une distension abdominale associée ŕ une sensation de pesanteur pelvienne, une douleur basithoracique droite ŕ type de point de côté, une toux sčche et une dyspnée d'effort. Le tout évoluait dans un contexte de fléchissement l'état général. L'examen clinique retrouvait un syndrome d'épanchement liquidien des deux tiers inférieurs de l'hémithorax droit, une distension abdominale avec une matité diffuse et un signe de flot positif, une masse abdomino-pelvienne qui mesurait douze centimčtres de diamčtre, ferme, latéralisée ŕ droite par rapport ŕ l'utérus, avec un signe de glaçon positif. Le téléthorax montrait une opacité de type pleural occupant les deux tiers inferieurs de l'hémithorax droit (Figure 1). La ponction pleurale montrait un liquide jaune citrin exsudatif, lymphocytaire. Trois ponctions biopsies pleurales montraient un remaniement inflammatoire chronique non spécifique, sans signes de malignité. L'étude cytodiagnostique du liquide pleural n'avait pas montré de cellules malignes. La pleurésie récidivait aprčs plusieurs ponctions évacuatrices. L'échographie abdominopelvienne montrait une ascite de grande abondance anéchogčne et libre, une masse solidokystique latéro-utérine droite, ŕ priori ovarienne, mesurant 14 x 12 centimčtres. La tomodensitométrie thoraco-abdomino-pelvienne montrait une masse ovarienne droite solidokystique qui mesurait 143 x 114 x 83 mm (Figure 2), des épanchements pleural droit et abdominal de grande abondance. Il n'existait pas de lésions parenchymateuses pulmonaires, ni d'adénopathies médiastinales, iliaques ou lombo-aortiques. Le dosage sérique du CA-125 était élevé ŕ 161 UI/mL pour une normale inférieure ŕ 35 UI/mL. Une laparotomie diagnostique et thérapeutique était indiquée. L'exploration chirurgicale retrouvait une ascite de grande abondance de trois litres qui était aspirée, un ovaire droit sičge d'une tumeur de 16x14 centimčtres (Figure 3), Il n'existait pas de nodules péritonéaux, épiploďques ou hépatiques, ni d'adénopathies pelviennes ou lomboaortiques palpables. Une biopsie tumorale était examinée histologiquement en extemporanée objectivant un processus tumoral malin. Une hystérectomie totale sans conservation annexielle, un curage ganglionnaire pelvien et lombo-aortique, une omentectomie, des biopsies péritonéales et pariétales et un prélčvement du liquide d'ascite étaient réalisés. L'examen anatomopathologique de la pičce opératoire montrait un cystadénocarcinome séreux, unilatéral de l'ovaire droit essentiellement solide avec effraction capsulaire. L'ovaire controlatéral était normal. Il n'existait pas de métastase ganglionnaire, omentales, péritonéales ou pariétales. Le cytodiagnostic du liquide d'ascite ne montrait pas de cellules malignes. Le cancer ovarien était classée stade Ic de la FIGO (fédération internationale de gynécologie-obstétrique). Les suites opératoires étaient simples. Des contrôles cliniques, radiologiques (Figure 4) et échographiques réalisés une semaine, deux semaines, un mois et deux mois aprčs l'intervention et avant de démarrer la chimiothérapie ne montraient pas d'épanchement pleural ni péritonéal. La régression de la pleurésie et l'ascite était spectaculaire, immédiatement aprčs l'exérčse chirurgicale et en absence de toute chimiothérapie. La patiente n'avait pas reçu de chimiothérapie par refus de celle-ci. Des contrôles sériques du CA 125, réalisés dix jours puis un mois aprčs l'intervention, étaient respectivement ŕ 16 et 12 UI/mL. Avec un recul de douze mois, aucune récidive n'était notée.
Le syndrome de Demons-Meigs comprend une tumeur ovarienne bénigne, associée ŕ une ascite et une pleurésie le plus souvent droite, dont l'exérčse entraine la disparition des épanchements. Il est le plus souvent décrit avec les fibrothécomes ou les tumeurs de la granulosa .En 1884, Albert Demons, médecin français, décrit l'association d'un kyste ovarien ŕ un épanchement pleural et péritonéale. En 1902, cette association des épanchements était rapportée avec les tumeurs solides de l'ovaire, les myomes du ligament large et les fibromes utérins. En 1904, premičre thčse de médecine faite par Codet-Boisse, élčve de Demons, rapportant une série de 16 cas, insiste sur l'association d'un fibrome ovarien ŕ des épanchements pleural et abdominal. En 1954, Meigs rapporte une série de 84 cas de fibromes de l'ovaire. Un peu plus tard, Funk Bruntano, le décrit avec les fibrothécomes, les tumeurs de la granulosa et les tumeurs de Brenner. Par la suite des cas sont rapportés avec toutes les tumeurs de l'appareil génital féminin [2]. Il est exceptionnellement décrit la disparition des épanchements aprčs l'exérčse d'une tumeur pelvienne maligne aussi avant toute chimiothérapie. Ce constat ramčne les auteurs ŕ définir une forme particuličre du syndrome de Demons-Meigs, le pseudo-Meigs syndrome, une dénomination ŕ part qui regroupe toutes les autres entités (tumeurs malignes sans cellules néoplasiques dans les épanchements, pseudotumeurs, et autres raretés). Weise et al. [3] ont décrit ce syndrome avec des léiomyomes utérins. Sunitha et al [1] l'ont décrit avec des angioléimyomes utérins. D'autres l'ont décrit avec des tumeurs ovariennes malignes primitives notamment des adénocarcinomes ou des carcinomes endométroďdes, ou bien secondaires métastatiques [4]. Elizabeth et al. [5] ont rapporté ce syndrome avec des cancers digestifs notamment colorectaux. Par ailleurs, d'autres auteurs incluent sous le nom du pseudo-Meigs syndrome, toute tumeur bénigne du tractus génital associée ŕ une pleurésie et une ascite, et de ce fait, ils ont exclus toutes tumeurs malignes pelviennes de ce syndrome [6].
La physiopathologie est encore discutée et reste hypothétique. Une théorie mécanique suggčre la persistance du canal pleuropéritonéal et le rôle des troncs lymphatiques transdiaphragmatiques dont la compression tumorale entraine l'ascite qui transsude ŕ travers ce canal pour donner la pleurésie [2]. Mais cette théorie n'explique pas les observations décrites du syndrome en cas de tumeurs de petite taille, parfois millimétriques. La théorie hormonale suggčre un dérčglement endocrinien d'une tumeur sécrétante les'strogčnes ŕ point de départ génital. En effet, des thécomes minimes ou une hyperplasie thécale est retrouvée ŕ l'examen histologique minutieux de toutes les tumeurs ovariennes accompagnant ce syndrome (fibrome, kyste, goitres ovariens, cystadénocarcinome ..) ou męme lors de certains états physiologiques (ovulation, grossesses, début de ménopause) [7].
Les CA 125 sériques, marqueurs antigéniques de l'épithélium coelomique et de ses dérivés, ne sont pas spécifiques des tumeurs ovariennes. Il est classique au cours de ce syndrome de mettre en évidence une élévation du CA 125 [7], Un taux élevé n'est pas un bon indicateur de malignité ovarienne et peut ętre en rapport avec la quantité de l'épanchement ascitique, elle-męme en rapport avec la taille tumorale [7-11]. Dans notre observation, quoiqu'il s'agisse d'une tumeur maligne, le taux du CA 125 n'était pas trčs élevé que ce que le voudrait un cancer ovarien métastatique.
L'association d'un cystadénocarcinome ovarien avec une pleurésie et une ascite plaiderait plutôt en faveur de l'origine métastatique de ces épanchements. En revanche, la négativité des ponctions biopsies pleurales, des biopsies péritonéales, épiploďques et ganglionnaires, l'absence de cellules malignes sur les études cytodiagnostiques du liquide pleural et péritonéale et la disparition de ces épanchements aprčs l'exérčse chirurgicale de la tumeur et avant toute chimiothérapie, plaideraient en faveur d'un pseudo-syndrome de Meigs.
Le pseudo-Meigs syndrome est une entité rare, sa physiopathologie reste obscure .Le critčre majeur repose sur l'exclusion de l'origine métastatique des épanchements pleural et péritonéal, et leur disparition aprčs l'exérčse tumorale de la tumeur pelvienne et avant toute chimiothérapie. Une telle distinction est importante aussi bien sur le plan thérapeutique que pronostique.
Les auteurs ne déclarent aucun conflit d’'intéręts
Tous les auteurs ont contribué a la rédaction de ce manuscrit et ont lu et approuvé la version finale.
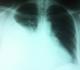
Figure 1: Radio du thorax montrant une opacité de type pleural occupant les deux tiers inférieurs de l’hémithorax droit
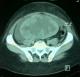
Figure 2: Coupe tomodensitométrique pelvienne montrant une masse ovarienne droite solidokystique qui mesurait 143 x 114 x 83 mm
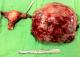
Figure 3: Exploration chirurgicale montrant un ovaire droit sičge d’une tumeur de 16x14 centimčtres
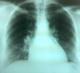
Figure 4: Radio du thorax réalisée deux mois aprčs la chirurgie montrant un assčchement total de la pleurésie droite
- Thomas S, Radhakrishnan L, Abraham L, Matthai A. Uterine Angioleiomyoma with Atypia, Raised CA-125 Levels, and Pseudo-Meigs Syndrome: An Alarming Presentation. Case Reports Pathol 2012.2012;519473 PubMed | Google Scholar
- Boufettal H, Zaghba N, Morad S, Bakhatar A, Yassine N, Bahlaoui A, et al. Syndrome de Demons-Meigs. Rev Pneumol Clin. 2011;67(2):121-3 PubMed | Google Scholar
- Weise M, Westphalen S, Fayyazi A, Emons G, Krauss T. Pseudo-Meigs syndrome: uterine leiomyoma with bladder attachment associated with ascites and hydrothorax-a rare case of a rare syndrome. Onkologie 2002;25(5): 443-6. PubMed | Google Scholar
- Fujii M, Okino M, Fujioka K, Yamashita K, Hamano K. Pseudo-Meigs' syndrome caused by breast cancer metastasis to both ovaries. Breast Cancer. 2006; 13(4):344-348 PubMed | Google Scholar
- Elizabeth DF, Hughes MS, Stratton P, Schrump DS, Alexander Jr HR. Pseudo-Meigs syndrome secondary to isolated colorectal metastasis to ovary: a case report and review of the literature. Gynecol Oncol.2004;93(1):248-251. PubMed | Google Scholar
- Brun GH. Syndromes et pseudosydromes de Demons et Meigs aujourd'hui. J Gynecol Obstet Biol Reprod. 2010 ; 39(3) :191-195 PubMed | Google Scholar
- Peyron N, Coulon A. Struma ovarii, pseudo-Meigs' syndrome and raised CA125, a rare association, Answer to May e-quid. Diagn Interv Imaging. 2012;93(7-8):643 PubMed | Google Scholar
- Chen YY, Hsiao SM, Hsu YP, Lin HH, Wei MC. Borderline mucinous ovarian tumor presenting as pseudo-Meigs' syndrome. J Obstet Gynaecol Res. 2013;39(1):434-6 PubMed | Google Scholar
- Quinlan DJ. Meigs' syndrome. J Obstet Gynaecol Can. 2012;34(4):311 PubMed | Google Scholar
- Moran-Mendoza A, Alvarado-Luna G, Calderillo-Ruiz G, Serrano-Olvera A, Lopez-Graniel CM, Gallardo-Rincon D. Elevated CA125 level associated with Meigs' syndrome: case report and review of the literature. Int J Gynecol Cancer. 2006;16(1):315-8 PubMed | Google Scholar
- Bethune M, Quinn M, Rome R. Struma ovarii presenting as acute pseudo-Meigs syndrome with an elevated CA 125 level. Aust N Z J Obstet Gynaecol. 1996; 36(3): 372-373 PubMed | Google Scholar