La tuberculose abdominale pseudo-tumorale
Rachid El Barni, Mohamed Lahkim, Abdessamad Achour
Corresponding author: Rachid El Barni, Service de chirurgie générale. Hôpital militaire Avicenne, Marrakech, Maroc 
Received: 10 Sep 2012 - Accepted: 01 Oct 2012 - Published: 15 Oct 2012
Domain: Clinical medicine
Keywords: Tuberculose, pseudo-tumorale, abdomen
©Rachid El Barni et al. Pan African Medical Journal (ISSN: 1937-8688). This is an Open Access article distributed under the terms of the Creative Commons Attribution International 4.0 License (https://creativecommons.org/licenses/by/4.0/), which permits unrestricted use, distribution, and reproduction in any medium, provided the original work is properly cited.
Cite this article: Rachid El Barni et al. La tuberculose abdominale pseudo-tumorale. Pan African Medical Journal. 2012;13:32. [doi: 10.11604/pamj.2012.13.32.2028]
Available online at: https://www.panafrican-med-journal.com//content/article/13/32/full
La tuberculose abdominale pseudo-tumorale
Rachid El Barni1,&, Mohamed Lahkim1, Abdessamad Achour1
1Service de chirurgie générale. Hôpital militaire Avicenne, Marrakech, Maroc
&Auteur correspondant
Rachid El Barni, Service de chirurgie générale. Hôpital militaire Avicenne, Marrakech, Maroc
La tuberculose extra-pulmonaire représente prčs de 1/3 des cas de tuberculose déclarés au Maroc [1]. Elle sičge par ordre de fréquence décroissant, au niveau ganglionnaire, génito-urinaire, ostéo-articulaire et neuro-méningé [2]. La localisation abdominale est relativement fréquente et représente 5 ŕ 10 % de l’ensemble des localisations [3].
La symptomatologie est non spécifique et la palpation d’une masse abdominale peut orienter ŕ tort vers une pathologie tumorale maligne, d’autant plus que la symptomatologie évolue dans un contexte d’altération de l’état général. Ce diagnostic, difficile et fréquemment méconnu, doit ętre évoqué surtout si le contexte épidémiologique s’y pręte [3], en présence d’une atteinte pulmonaire concomitante, ou devant des antécédents de tuberculose.
Les formes pseudo-tumorales de la tuberculose abdominale sont rarement rapportées dans la littérature, engendrant un retard diagnostique et par conséquent la persistance de l’évolutivité de cette maladie normalement curable. Les auteurs ont donc jugé utile de rapporter cinq cas de tuberculose abdominale pseudo-tumorale et d’en souligner les aspects diagnostiques et thérapeutiques.
Observation 1
NW. S, âgé de 18 ans, sans antécédents pathologiques particuliers, avait présenté depuis trois jours des douleurs abdominales diffuses et maximales en péri-ombilical sans syndrome occlusif. A son admission, le patient était fébrile ŕ 39°, son état hémodynamique était stable. La palpation abdominale trouvait une sensibilité abdominale diffuse avec une défense para-ombilicale droite. Le toucher rectal était indolore et le doigtier revenait propre.
Le taux des globules blancs était ŕ 19 500 éléments/mm3. Une radiographie de l’abdomen sans préparation objectivait une aérocolie. L’échographie abdominale trouvait un épanchement péri-cćco-appendiculaire et au niveau du douglas sans épaississement appendiculaire.
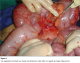
Une laparotomie exploratrice avait été décidée et qui avait trouvé un appendice normal, un épanchement péritonéal séreux de moyenne abondance avec une masse dure mal limitée au niveau du méso côlon en regard de l’angle colique droit (Figure 1). Ŕ son ouverture, cette masse avait un contenu purulent et une coque épaisse. Un prélčvement du pus, des biopsies multiples de la coque, une toilette et un drainage de la cavité abcédée ont été réalisés. Les suites opératoires ont été simples et l’examen anatomo-pathologique des biopsies de la coque revenait en faveur d’une tuberculose péritonéale. Une chimiothérapie anti-tuberculeuse a été instaurée et l’évolution était favorable au bout de deux mois.
Observation 2
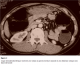
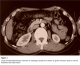
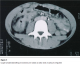
M.O, âgé de 42 ans, ayant comme antécédent pathologique un tabagisme chronique, souffrait depuis trois semaines de douleurs épigastriques associées ŕ un syndrome subocclusif avec fičvre et altération de l’état général. L’examen clinique trouvait un patient fébrile ŕ 38,5° avec présence d’une masse épigastrique ferme et sensible. La biologie montrait un syndrome inflammatoire non spécifique et une hyperleucocytose ŕ 12 700 éléments blancs/mm3. La tomodensitométrie (TDM) abdominale objectivait une masse ovalaire d’environ 10 cm de grand axe, comportant quelques images arrondies de tailles variables spontanément hypodenses et se rehaussant de façon hétérogčne. Cette masse attenante au grand omentum, était associée ŕ une distension colique avec stase stercorale (Figure 2). Elle avait orienté, du fait de son aspect et de son sičge vers une tumeur du grand omentum de type tumeur stromale, mésothélium malin ou tuberculose dans sa forme pseudo-tumorale. L’intradermo-réaction (IDR) ŕ la tuberculine était faiblement positive. Une ponction scano-guidée a était réalisée et l’examen anatomo-pathologique avait conclu a un aspect morphologique vaguement granulomateux avec nécrose caséiforme soulevant le diagnostic de tuberculose. Une chimiothérapie anti-tuberculeuse a été instaurée et l’évolution clinique était bonne avec nettoyage complet de la lésion du grand omentum au bout de 3 mois de traitement anti-tuberculeux (Figure 3).
Observation 3
B.M, âgé de 23 ans, sans notion de contage tuberculeux, présentait depuis deux mois des douleurs abdominales diffuses avec trouble du transit ŕ type de diarrhée glaireuse sans rectorragie évoluant dans un contexte d’asthénie, d’anorexie et d’amaigrissement chiffré ŕ 10 kg. L’examen clinique ŕ l’admission trouvait un patient apyrétique en mauvais état général, avec un abdomen distendu et une sensibilité de la fosse iliaque gauche sans organomégalie et le toucher rectal était normal. Les aires ganglionnaires périphériques étaient libres. La radiographie du thorax avait montré une pacchypleurite axillaire droite avec scissurite. La radiographie de l’abdomen sans préparation trouvait une aérocolie sans niveau hydro-aérique. Un lavement ŕ la gastrografine a mis en évidence une lésion végétante étendue sur 4 cm et siégeant au niveau du côlon sigmoďde se raccordant en trognon de pomme avec le reste du côlon (Figure 4). La colonoscopie avait confirmé la présence d’une lésion ulcéro-bourgeonnante au niveau du côlon sigmoďde réduisant la lumičre colique et évoquant une tumeur colique dont la biopsie était en faveur d’une colite granulomateuse sans nécrose caséeuse ni signes de malignité. L’échographie abdominale avait montré un épanchement liquidien en interanses, et la TDM abdomino-pelvienne avait objectivé en plus une stase stercorale colique en rapport avec épaississement pariétal circonférentiel et irrégulier du sigmoďde. Les examens biologiques ont montré une anémie microcytaire ŕ 9,6 g/dl et un syndrome inflammatoire non spécifique. L’IDR ŕ la tuberculine et la recherche des mycobactéries dans les crachats étaient négatives. La sérologie HIV était négative et les marqueurs tumoraux (antigčne carcino-embryonnaire, antigčne carbo-hydrate 19-9) avaient des taux normaux.
Une laparotomie exploratrice était décidée. L’exploration chirurgicale avait trouvé un épanchement péritonéal séreux, des nodules péritonéaux et une distension colique en rapport avec une sténose du sigmoďde. Les gestes réalisés étaient une biopsie des nodules péritonéaux, une sigmoďdectomie avec anastomose colorectale. L’examen anatomo-pathologique des biopsies péritonéales et de la pičce de sigmoďdectomie était en faveur d’un processus inflammatoire granulomateux spécifique largement nécrosé évoquant une tuberculose. Les suites opératoires étaient simples. Une chimiothérapie anti-tuberculeuse a été préconisée pendant une année au bout de laquelle le patient avait repris du poids avec disparition de tous les signes cliniques.
Observation 4
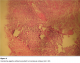
M.M, âgé de 26 ans, connu séropositif, était hospitalisé pour masse douloureuse de la fosse iliaque droite (FID) et des troubles du transit intestinal ŕ type d’alternance diarrhée-constipation évoluant depuis trois mois. L’examen abdominal avait trouvé une masse de la FID ferme, douloureuse, adhérente au plan profond et mobile par rapport au plan superficiel mesurant six cm de diamčtre. Le reste de l’examen clinique ne trouvait pas d’hépato-splénomégalie ni d’adénopathies périphériques et le toucher rectal était sans particularité. Le bilan biologique a révélé un syndrome inflammatoire non spécifique. L’échographie complétée par la TDM abdominale avaient montré une masse de la FID mesurant 5 × 6 cm ŕ structure solide, ŕ contours irréguliers, ŕ développement surtout intra-colique, et qui se rehaussait aprčs injection du produit de contraste (PC) (Figure 5). En outre, on notait l’absence d’ascite, d’adénopathies profondes et de lésions hépatiques. Devant cet aspect, l’origine néoplasique a été retenue et l’origine inflammatoire a été évoquée en dernier lieu. Les marqueurs tumoraux (ACE, AFP, CA 19-9) étaient normaux. Au cours de son hospitalisation, le patient avait présenté un syndrome subocclusif et une laparotomie était décidée en urgence et qui avait permis la réalisation d’une résection iléocćcale avec anastomose iléo-transverse termino-latérale. Les suites opératoires étaient marquées par une péritonite ŕ J+2 ayant nécessité une reprise chirurgicale et la réalisation d’une double stomie. Le patient était décédé ŕ J+3 dans un tableau de choc septique. L’examen anatomo-pathologique qui a conclu ŕ une tuberculose colique pseudo-tumorale (Figure 6).
Observation 5
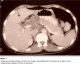
N. Z âgée de 38 ans, infirmičre, hospitalisée pour altération de l’état général évoluant depuis un an avec fičvre. L’examen clinique avait trouvé une patiente fébrile ŕ 38,5° et qui présentait une masse épigastrique ferme et sensible. La biologie avait montré un syndrome inflammatoire non spécifique et l’IDR ŕ la tuberculine était ŕ 12 mm. La TDM abdominale avait montré une image spontanément hypodense, se rehaussant en périphérie aprčs injection du PC, vraisemblablement nécrotique, centrée sur la région coelio-mésentérique, englobant l’isthme du pancréas et s’étendant au hile hépatique et ŕ l’arričre cavité des épiploons (Figure 7). Cette image était associée ŕ d’autres images de męme nature rétro-péritonéales, péri-aorto-caves et iliaques notamment ŕ droite. Cet aspect faisait discuter une hémopathie en premier lieu et en particulier un lymphome. Le diagnostic de tuberculose pseudo-tumorale avait été également évoqué. La biopsie d’une adénopathie iliaque droite était réalisée et l’examen anatomo-pathologique avait conclu ŕ une tuberculose ganglionnaire. L’évolution clinique était favorable au bout de 6 mois de chimiothérapie anti-tuberculeuse.
L’incidence de l’infection tuberculeuse a connu une ré-ascension non seulement dans les pays en voie de développement mais aussi dans les pays développés. Ceci est expliqué en partie par l’infection au virus de l’immunodéficience acquise (VIH), la précarité et l’immigration [2]. Ce qui a entrainé une augmentation de l’incidence des localisations extra-pulmonaires qui représentent prčs de 1/3 des cas de tuberculose déclarés au Maroc [1]. La localisation abdominale constitue une forme extra-pulmonaire relativement fréquente, elle représente 5 ŕ 10 % de l’ensemble des localisations [3]. Cette fréquence est plus importante et pourrait doubler ŕ tripler chez les sujets séropositifs. Elle a été estimée ŕ 13,5 % dans une étude faite sur 199 patients séropositifs [3,4]. Au cours de la tuberculose abdominale tous les organes peuvent ętre atteints, et les localisations les plus habituelles de la tuberculose digestive sont l’intestin gręle (44 %), le caecum (35 %) et l’iléo-caecum (16 %) [5]. L’atteinte isolée du côlon est rare, elle est estimée entre 2 et 9 % et dominée par l’atteinte du côlon droit [6]. Les autres localisations abdominales concernent les ganglions, le péritoine, le foie et la rate [7]. Il s’agit d’une localisation péritonéale dans la premičre observation, d’une localisation au niveau du grand omentum dans la deuxičme observation, d’une localisation péritonéale et sigmoďdienne qui est une association plus rare faisant la particularité de cette observation, d’une localisation colique droite chez le patient séropositif et d’une localisation ganglionnaire diffuse chez la seule patiente de l’étude.
L’atteinte digestive peut ętre primitive par ingestion directe de mycobactérium ou secondaire ŕ des lésions pulmonaires trčs bacillifčres par voie hématogčne ou lymphatique [8]. L’agent bactérien est le plus souvent le bacille de Kokh bovin ou humain, exceptionnellement ce sont les mycobactéries atypiques chez les sujets immunodéprimés [8]. La forme hypertrophique pseudo-tumorale serait le plus souvent primitive [7]. Cette forme touche l’adulte jeune entre 20 et 40 ans [10]. La prédominance féminine est retrouvée dans les localisations intestinales [11]. Dans nos observations, il s’agit de quatre hommes âgés successivement de 18 ans, 42 ans, 23 ans et 26 ans. Notre patiente était âgée de 38 ans.
La fréquence des formes pseudo-tumorales au cours de la tuberculose abdominale est difficile ŕ évaluer [2]. En effet, un aspect pseudo-tumoral n’est signalé que dans 5% des cas [3].
La symptomatologie des tuberculoses du tube digestif diffčre, bien entendu, de celle des tuberculoses péritonéales qui se manifestent par des douleurs abdominales et surtout une ascite [12,13]. C’est le cas de la premičre observation. Le tableau clinique de la tuberculose digestive est en général peu spécifique, se traduisant par un amaigrissement (80%), une fébricule (66%), un ballonnement abdominal douloureux (100%), une constipation (40%), une ascite (40 ŕ 100%), une diarrhée (15%) avec parfois un syndrome dysentérique en cas de localisation recto-sigmoďdienne, voire une forme pseudo-tumorale (5%) [14]. Des complications sont ŕ craindre dont la perforation, le plus souvent cloisonnée, l’occlusion, l’hémorragie ou la malabsorption en cas d’atteinte iléocćcale [14].
Les perturbations biologiques observées n’ont d’autre part rien de spécifique, qu’il s’agisse de l’anémie ou du syndrome inflammatoire. L’intradermo-réaction (IDR) ŕ la tuberculine n’est pas une preuve de la nature tuberculeuse de l’affection. La radiographie du thorax peut ętre utile pour attester de l’atteinte secondaire [1].
Les examens complémentaires sont d’une utilité limitée, sauf s’il existe une forte suspicion du diagnostic [15]. Les radiographies d’abdomen sans préparation dans les syndromes subocclusifs ou occlusifs ne font que confirmer l’existence d’un obstacle. Sur les opacifications du tube digestif, les sténoses (figure 4) ont la męme morphologie que celle que l’on peut observer dans la maladie de Crohn [3], diagnostic, ŕ priori, beaucoup plus probable dans les pays industrialisés [16]. Grâce ŕ l’échographie et ŕ la TDM, l’imagerie constitue une étape décisive quant au diagnostic des formes pseudo-tumorales [7]. L’atteinte intestinale, prédomine au carrefour iléocćcal et se présente comme des anses agglomérées, ŕ paroi épaissie de façon habituellement concentrique [7]. L’épaississement pariétal habituellement concentrique peut, quand il est excentré et ŕ développement exophytique extrinsčque, simuler plus une atteinte tumorale qu’une atteinte inflammatoire [7]. Cet épaississement peut ętre hétérogčne avec des foyers hypodenses en rapport avec de la nécrose caséeuse [7]. Le diagnostic de tuberculose reste difficile, et l’atteinte du carrefour iléocćcal peut simuler d’autres affections telles la maladie de Crohn, une néoplasie, ou une tumeur appendiculaire [7]. L’atteinte tuberculeuse peut aussi intéresser n’importe quel autre segment du tube digestif. Elle est souvent représentée par des anses agglutinées, une infiltration pariétale digestive hypertrophique avec des nodules péritonéaux, et un amas d’adénopathies profondes notamment mésentériques. Mais cet aspect peut manquer, et devant une infiltration digestive hypertrophique irréguličre excentrée, une origine tumorale est souvent évoquée [3]. La localisation ganglionnaire dans la tuberculose intra-abdominale peut également ętre ŕ l’origine de l’aspect pseudo-tumoral. Il peut s’agir d’un amas d’adénopathies de petite taille agglomérées satellites d’une atteinte digestive, péri-pancréatiques ou pédiculaires hépatiques comme le cas de la patiente de notre étude. Ce groupement pourtant spécifique de la tuberculose oriente plus souvent, du fait du sičge de la lésion vers une pathologie tumorale [17].
La tuberculose des organes pleins, dans sa forme hépato-splénique macro-nodulaire unique ou multiple, peut simuler pour une lésion tumorale maligne primitive ou secondaire [17]. Des formes exceptionnelles de tuberculose péritonéale telles la forme fibro-adhésive et la forme ulcéro-caséeuse peuvent aussi donner un aspect pseudo-tumoral [3]. La forme fibro-adhésive, pose quant ŕ elle le diagnostic différentiel avec les tumeurs carcinoďdes [7]. L’apport de l’IRM dans cette localisation abdominale est non spécifique, cet examen montre des lésions en hyposignal T1 avec un signal variable T2 au cours des localisations ganglionnaires et viscérales [7]. Devant un aspect hautement suggestif de l’imagerie, un bilan étiologique devrait ętre entamé pour dépister d’autres localisations pouvant conforter le diagnostic. Si le doute persiste une ponction guidée sous contrôle échographique ou scanographique avec étude histologique permettrait de poser le diagnostic [3].
En définitive, si l’urgence et la symptomatologie clinique permettent de les réaliser sans risque, les examens endoscopiques sont les plus utiles [18]. En effet, l’apport de l’endoscopie est essentiel, elle permet la détection des lésions, męme les plus superficielles [9,19]. Son intéręt majeur est qu’elle permet la réalisation de biopsies avec études histologique et bactériologique (culture) et évite alors la morbidité et la mortalité liées ŕ une laparotomie exploratrice [20,21]. La coloscopie peut montrer soit des érosions muqueuses, des ulcérations avec des zones nécrotico-hémorragiques, soit des zones de rétrécissement ou de sténose infranchissable avec des bourgeons autour [22]. Cependant, les biopsies per-endoscopiques ne sont pas toujours concluantes. Des colorations spécifiques (Ziehl-Nilson) et une mise en culture seront systématiquement réalisées (positive dans 42 ŕ 69 %) [20].
Plus récemment décrite, la recherche du BK par « polymerase chain reaction » (PCR) sur biopsies permet une forte sensibilité diagnostique (75 ŕ 80 %) et une spécificité élevée (85 ŕ 95 %) [20].
Savoir évoquer le diagnostic de tuberculose est la condition indispensable pour une prise en charge rapide et adaptée, car le pronostic vital est mis en jeu [3]. La laparotomie reste parfois le seul recours en cas de négativité de la ponction écho ou scano-guidée [3]. En effet, 20 ŕ 40% des malades [6] subiront une laparotomie, soit en urgence devant une complication (sténose, occlusion, masse compressive, mise ŕ plat de certaines cavités caséifiées, perforation et fistule), soit dans un but diagnostique. Le traitement percutané peut ętre proposé en cas de formes abcédées [23].
Le traitement chirurgical n’est pas standardisé et dépend d’abord du motif de l’indication opératoire. Ainsi, la levée d’un ou de plusieurs obstacles en cas d’occlusion ou un procédé d’hémostase en cas d’hémorragie massive vont rendre habituellement nécessaire une résection. Il dépend aussi et surtout des lésions constatées ŕ l’exploration chirurgicale et qui impliquent le plus souvent des résections intestinales avec ou sans rétablissement de la continuité ou des dérivations internes ou des stomies. Le choix d’une résection doit toujours prendre en compte l’étendue de la résection. Si elle devait ętre trop étendue, surtout au niveau de l’iléon, des stomies doivent ętre préférées en comptant sur le traitement antituberculeux pour réduire l’étendue de résections secondaires qui seraient nécessaires [24]. Les constatations per-opératoires ne permettent pas toujours de reconnaître la nature tuberculeuse de ces formes pseudo-tumorales et le diagnostic ne sera définitivement posé qu’aprčs examen histologique de la pičce opératoire [1].
Ce traitement chirurgical doit ętre associé ŕ un traitement antituberculeux et c’est le cas de tous nos patients. La nature des complications postopératoires ne diffčre pas de celle que l’on peut observer dans d’autres indications. En revanche, leur fréquence élevée comme la mortalité postopératoire s’expliquent par le fait qu’il s’agisse de malades tuberculeux, venant souvent consulter tardivement, dans un état général trčs altéré [24].
La tuberculose abdominale pseudo-tumorale, rare męme en pays d’endémie comme le notre, pose un grand problčme diagnostique notamment avec le cancer. Ce qui justifie souvent le recours ŕ une laparotomie chaque fois que persiste un doute diagnostique ou encore en cas de complication.
Les auteurs ne déclarent aucun conflit d’intéręt.
Tous les auteurs ont contribué ŕ la rédaction de ce manuscrit et lu et approuvé la version finale.
Figure 1: Vue opératoire montrant une masse mal limitée du méso côlon en regard de l’angle colique droit
Figure 2: Coupe tomodensitométrique montrant une masse du grand omentum associée ŕ une distension colique avec stase stercorale
Figure 3: Coupe tomodensitométrique montrant un nettoyage complet de la lésion du grand omentum aprčs 3 mois de traitement anti-tuberculeux
Figure 4: Lavement ŕ la gastrografine montrant un aspect en «trognon de pomme» du côlon sigmoďde
Figure 5: Coupe tomodensitométrique montrant une masse du côlon droit ŕ contours irréguliers
Figure 6: Granulome giganto-cellulaire jouxtant la musculeuse colique (HE X 40)
Figure 7: Coupe tomodensitométrique montrant une image vraisemblablement nécrotique de la région coelio-mésentérique englobant l’isthme du pancréas
- Ismaďli Z, Amraoui M, Mansouri F, Essamri W, Benazzouz M, Essaďd EA. Tuberculose colique pseudo-tumorale ŕ double localisation. Médecine du Maghreb. 2006; 142: 5-8.
- Denis-Delperre N, Merrien D, Billaud E et al. Tuberculose extra-pulmonaire dans la région du centre-ouest: Étude rétrospective de 217 cas (GERICCO 199161993). Presse Med. 1998 Feb 28;27(8):341-6. This article on PubMed
- Romand F, Gaudin JL, Bobinchon R, Souquet JC. Tuberculose abdominale d’allure pseudo tumorale. Presse Med. 1997 Nov 22;26(36):1717-21. This article on PubMed
- Verspyck E, Struder C, Wendum D, Bourgeois D, Lariven S, Marpeau L. Tuberculose péritonéale. Ann chir. 1997; 51: 375-78. This article on PubMed
- Barbier JP. Tuberculose intestinale. Encycl Méd Chir (Elsevier, Paris) Estomac-intestin. 1975; 9060 A10.
- Badre W et Coll. Tuberculose digestive pseudo-tumorale. Magh Med. 2002; 22(363): 208-11.
- Hablani N, Souei Mhiri M, Tlili Graies K, Jemni Gharbi H, Abdallah S et Bel Hadj Hamida R. La tuberculose abdominale pseudo-tumorale A propos de 4 observations. J Radiol. 2005; 86: 1021-5. This article on PubMed
- De Jesus LE, Marques AM, Rocha MS, et al. Left colon stenosis caused by tuberculosis. J Pediatr Surg. 2004; 39: e5-e7. This article on PubMed
- Misra SP, Misra V, Dwivedi M, Gupta SC. Colonic tuberculosis : clinical features, endoscopic appearance and management. J Gastroenterol Hepatol. 1999 Jul;14(7):723-9. This article on PubMed
- Ibrarallah M, Mohan A, Sakari A, Srinivas M, Mishra A. Abdominal tuberculosis : diagnosis by laparoscopy and colonoscopy. Trop gastroenterol. 2002; 23(3): 150-3. This article on PubMed
- Marshall JB et coll. Tuberculosis of the gastrointestinal tract and peritoneum. Am J Gastroenterol. 1993 Jul;88(7):989-99. This article on PubMed
- Tanrikulu AC, Aldemir M, Gurkan F, Suner A, Dagli CE, Ece A. Clinical review of tuberculous pritonitis in 39 patients in Diyarbakir, Turkey.J Gastroenterol Hepatol. 2005 Jun;20(6):906-9. This article on PubMed
- Thoreau N, Fain O, Babinet P, Lortholary O, Valeyre D, Boudon P, et al. Tuberculose péritonéale : 23 cas dans la banlieue nord-est de Paris. Int J Tuberc Lung Dis. 2002; 6: 253-8. This article on PubMed
- Kaplanski G, Granel B, Payan MJ, Sielezneff I, Folchetti G, Durand JM, et al. Pseudodiverticulite sigmoďdienne fistulisée d’origine tuberculeuse. Rev Med Interne. 1998 Jun;19(6):447-8. This article on PubMed
- Vanhoenacker FM, De Backer AI, de BB O, Maes M, Van Altea R, Van Beeckvoort D, et al. Imaging of gastro-intestinal and abdominal tuberculosis. Eur Radiol. 2004; 14(suppl 3): E103-E115. This article on PubMed
- Collado C, Stirnemann J, Ganne N, Trinchet JC, Cruaud P, Barrat C, et al. Gastrointestinal tuberculosis: 17 cases collected in 4 hospitals in the northeastern suburb of Paris. Gastroenterol Clin Biol. 2005; 29: 419-24. This article on PubMed
- Jemni H, Bellara I, Tlili K et al. Lymphadénite mésentérique d’origine tuberculeuse: A propos d’un cas. J Radiol. 2000; 81: 1715-7. This article on PubMed
- Martinez Tirado P, Loez De Hierro Ruiz M, Martinez Garcia R, Martinez Cara JG, Martin Rodriguez MM, Castilla castellano MM. Intestinal tuberculosis A diagnostic challenge. Gastroenterol Hepatol. 2004; 27: 43-4. This article on PubMed
- Isaacs P, Zissis M. Colonic tuberculosis and adenocarcinoma : an unusual presentation. Eur J Gastroenterol Hepatol. 1997 Sep;9(9):913-5. This article on PubMed
- Florent C Rambaud JC. Traité de gastro-entérologie. Tuberculose digestive. 2000; 983-7.
- Kacem C, Kamoun A, Bahout M, Zermani R, Najjar T. Colonic tuberculosis : an exceptional cause of a massive surgical hemorrhage a propos of a case and review of the literature. Tunis Med. 1999; 77(10): 530-3. This article on PubMed
- Jamil D, Ismaďl R, Bellabah A, Alaoui R, Cherkaoui A. La tuberculose du côlon transverse A propos de 2 observations. Ann Gastroenterol Hepatol (Paris). 1992 Jan-Feb;28(1):21-4. This article on PubMed
- Renier JF, Paladines G, Lesur G, et al. Tuberculose sigmoďdienne abcédée et isolée. Presse Med. 1991; 20: 1230-1. This article on PubMed
- Nguyen Duc C, Pha Hai B, Pham Van T, Ton That B, Huguier M. Tuberculoses compliquées du tube digestif. Annales de chirurgie. 2006; 131: 306-10. This article on PubMed